Процесс горения зависит от множества условий, главнейшим из которых являются:
· состав горючей смеси;
· давление в зоне горения;
· температура реакции;
· геометрические размеры системы;
· агрегатное состояние горючего и окислителя и др.
В зависимости от агрегатного состояния горючего и окислителя различают следующие виды горения:
· гомогенное;
· гетерогенное;
· горение ВВ.
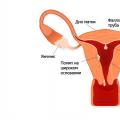
Гомогенное горение происходит в газо- или парообразных горючих системах (рис. 1.1) (горючее и окислитель равномерно перемешаны друг с другом).
Так как парциальное давление кислорода в зоне горения (равно) близко к нулю – кислород довольно свободно проникает к зоне горения (практически он находится в ней), поэтому скорость горения определяется главным образом скоростью протекания химической реакции, увеличивающейся с ростом температуры. Такое горение (или горение таких систем) называется кинетическим.
Рис.1.1. Схема процесса горения паров или газов
Полное время сгорания в общем случае определяется по формуле
t р = t Ф + t Х,
где t Ф – время физической стадии процесса (диффузии О 2 к очагу через слой); t Х – время протекания химической стадии (реакции).
При горении однородных систем (смеси паров, газов с воздухом) время физической стадии процесса несоизмеримо меньше скорости протекания химической реакций, поэтому t Р » t Х – скорость определяется кинетикой химической реакции и горение называется кинетическим.
При горении химически неоднородных систем время проникновения О 2 к горючему веществу сквозь продукты сгорания (диффузия) несоизмеримо больше времени протекания химической реакции, таким образом определяет общую скорость процесса, т.е. t Р » t Ф. Такое горение называется диффузионным.
Примерами диффузионного горения (рис. 1.2) является горение каменного угля, кокса (продукты горения препятствуют диффузии кислорода в зону горения)

Рис.1.2. Схема диффузии кислорода в зону горения твердого вещества
(гетерогенное горение)
Концентрация кислорода в объеме воздуха С 1 значительно больше его концентрации вблизи зоны горения С 0 . При отсутствии достаточного количество О 2 в зоне горения химическая реакция тормозится (и определяется скоростью диффузии).
Если продолжительность химической реакции и физической стадии процесса соизмеримы, то горение протекает в промежуточной области (на скорость горения влияют как физические, так и химические факторы).
При низких температурах скорость реакции слабо зависит от температуры (кривая медленно поднимается вверх). При высоких температурах скорость реакции сильно увеличивается (т.е. скорость реакции в кинетической области зависит главным образом от температуры реагирующих веществ).
Скорость реакции окисления (горения) в диффузионной области определяется скоростью диффузии и очень мало зависит от температуры. Точка А – переход из кинетической в диффузионную область (рис.1.3).
Процесс горения всех веществ и материалов независимо от их агрегатного состояния происходит, как правило, в газовой фазе (жидкость – испаряется, твердые горючие вещества выделяют летучие продукты). Но горение твердых веществ имеет многостадийный характер. Под воздействием тепла – нагрев твердой фазы – разложение и выделение газообразных продуктов (деструкция, летучие вещества) – сгорание – тепло нагревает поверхность твердого вещества – поступление новой порции горючих газов (продуктов деструкции) – горение.

Рис. 1.3. Зависимость скорости V кинетического (1)
и диффузионного (2) от температуры. Точка А – переход
из кинетической области в диффузионную
Многие твердые горючие вещества (древесина, хлопок, солома, полимеры) в своем составе имеют кислород. Поэтому для их сгорания требуется меньший объем кислорода воздуха. А горение взрывчатого вещества (ВВ) практически вообще не нуждается во внешнем окислителе.
Таким образом, горение ВВ – это самораспространение зоны экзотермической реакции его разложения или взаимодействие его компонентов путем передачи тепла от слоя к слою.
Горючие системы могут быть химически однородными и неоднородными. К химически однородным относятся системы, в которых горючее вещество и воздух равномерно перемешаны: смеси горючих газов, паров или пылей с воздухом. К химически
неоднородным относятся системы, в которых горючее вещество и воздух не перемешаны и имеют поверхности раздела: твердые горючие материалы и жидкости, находящиеся в воздухе, струи горючих газов и паров, поступающие в воздух и т.д.
Примером горения газов и паров (гомогенное горение) является горение паров, поднимающихся со свободной поверхности жидкости (рис. 1.1) или горение газа, выходящего из трубы. Так как парциальное давление кислорода воздуха равно 21,2 кПа, а в зоне горения давление равно нулю, кислород из воздуха диффундирует через слой продуктов сгорания к зоне горения. Следовательно, скорость реакции горения зависит от скорости диффузии кислорода.
Примером горения на поверхности твердого вещества (гетерогенное горение) является горение антрацита, кокса, древесного угля. В этом случае диффузии кислорода к зоне горения также препятствуют продукты сгорания, что видно из схемы, показанной на рис. 1.2. Концентрация кислорода в объеме воздуха (С 1) значительно больше концентрации его вблизи зоны горения (С 0). В отсутствие достаточного количества кислорода в зоне горения химическая реакция тормозится.

Рис. 1.2. Схема диффузии кислорода в зону горения твердого вещества
(гетерогенное горение)
Таким образом, полное время сгорания химически неоднородной горючей системы складывается из времени, необходимого для возникновения физического контакта
между горючим веществом и кислородом воздуха , и времени, затрачиваемого на протекание самой химической реакции :
В случае гомогенного горения величина называется временем смесеобразования, а в случае гетерогенного горения – временем транспортировки кислорода из воздуха к твердой поверхности горения.
В зависимости от соотношения и горение называется диффузионным или кинетическим. При горении химически неоднородных горючих систем время диффузии кислорода к горючему веществу несоизмеримо больше времени, необходимого для протекания химической реакции, т.е. >> и практически .
Это значит, что скорость горения определяется скоростью диффузии кислорода к горючему веществу. В этом случае говорят, что процесс протекает в диффузионной области. Такое горение и называется диффузионным. Все пожары представляют собой диффузионное горение.
Если время физической стадии процесса оказывается несоизмеримо меньше времени, необходимого для протекания химической реакции, т.е. << , то можно принять . Скорость процесса практически определяется только скоростью химической реакции. Такое горение называется кинетическим. Так горят химически однородные горючие системы, в которых молекулы кислорода хорошо перемешаны с молекулами горючего вещества, и не затрачивается время на смесеприготовление. Так как скорость химической реакции при высокой температуре велика, горение таких смесей происходит мгновенно и носит характер взрыва. Если продолжительность химической реакции и физическая стадия процесса горения соизмеримы, то горение протекает в так называемой промежуточной области, в которой на скорость горения влияют как химические, так и физические факторы.
На рис. 1.3 показана зависимость скорости реакции горения от температуры в различных областях. Кривая 1 показывает изменение скорости реакции при кинетическом горении. При низких температурах скорость реакции окисления в смеси слабо зависит от изменения температуры, и кривая 1 на этом участке медленно поднимается вверх. При более высоких температурах скорость реакция окисления начинает сильно ускоряться с повышением температуры, и кривая 1 круто поднимается. Таким образом, скорость реакции в кинетической области зависит только от температуры реагирующих веществ.

Рис. 1.3. Зависимость скорости кинетического (1) и диффузионного (2)
горения от температуры
Кривая 2 показывает изменение скорости реакции при диффузном горении. При низких температурах ход кривой 2 одинаков с кривой 1 , так скорость реакции окисления меньше скорости диффузии кислорода в зону горения и, следовательно, реакция протекает в кинетической области. При повышении температуры реагирующих веществ скорость реакции становится равной скорости диффузии кислорода в зону горения, а затем значительно превышает ее. В этих условиях скорость всего процесса определяется скоростью диффузии кислорода. Кривая 2 в точке А изменяет свое направление, отклоняясь вправо от кривой 1 . Дальнейший ход кривой 2 показывает, что скорость процесса горения в диффузионной области, определяемая скоростью диффузии, очень мало зависит от температуры.
В случае, когда через горелку подается только газ , горение происходит за счет взаимодействия газа с кислородом из окружающего воздуха. Поскольку горение происходит в процессе взаимной диффузии горючего и окислителя, подобное горение называется диффузионным горение . Скорость горения определяется интенсивностью процесса смешения горючего и окислителя. В зависимости от характера смешения различают ламинарное и турбулентное диффузионное горение.
Ламинарное диффузионное горение происходит при ламинарном режиме движения газа, вытекающего из горелки. Зона устойчивого горения устанавливается по поверхности, где горючее и окислитель находятся в стехиометрическом соотношении . Образующиеся продукты горения диффундируют как в окружающее пространство, так и внутри факела. Структура диффузионного ламинарного факела при сжигании водорода показана на рис. 3.19. Концентрация горючего падает от наибольшего значения на оси струи до нуля во фронте пламени, а концентрация кислорода возрастает от нуля во фронте пламени до его значения в окружающем потоке. Концентрация продуктов Н 2 О и температура Т максимальны во фронте пламени.
Рисунок 3.19 - Структура диффузионного ламинарного пламени при сжигании водорода
В диффузионном ламинарном пламени температура достигает максимального значения в зоне горения . Вытекающий из горелки газ нагревается за счет тепла, переносимого теплопроводностью и диффузией до поступления в зону горения.
В случае сжигания углеводородов их нагрев приводит к термическому разложению с образованием сажи и водорода . Находящиеся в пламени мелкодисперсные частицы сажи и свободного углерода, раскалившись, вызывают свечение пламени . Диффузионное горение частиц сажи протекает сравнительно медленно, в результате чего может возникнуть недожог топлива .
Высота ламинарного диффузионного пламени может быть рассчитана по формуле
где W – скорость истечения газа;
R – радиус соплового отверстия;
D – коэффициент молекулярной диффузии.
Интенсивность диффузионного сжигания зависит от интенсивности образования смеси.
Для промышленных условий более важным является способ турбулентного диффузионного горения , поскольку массообмен в пламени интенсивнее. С увеличением скорости размеры факела растут, достигая максимума. Одновременно теряется правильность очертаний и стабильность его вершины, начинается турбулизация факела , захватывающая все большую его длину. По мере приближения турбулентного фронта к корню факела высота его несколько снижается , оставаясь дальше постоянной. По достижении критической скорости газовой струи весь факел становится турбулентным, и в дальнейшем при увеличении скорости высота факела не изменяется. Относительная высота турбулентного диффузионного факела рассчитывается по формуле
где h – длина факела;
d – диаметр устья горелки;
Кинетическое горение – горение предварительно перемешанной смеси горючего и окислителя.
В этом случае пламя по горючей смеси будет распространяться во все стороны. Объем, охваченный пламенем, будет увеличиваться. Пламя всегда распространяется в сторону несгоревшей смеси.
Рис. 7.1. Схема распространения пламени по предварительно перемешанной гомогенной смеси: 1 – исходная горючая смесь; 2 – фронт пламени; 3 - продукты горения; d ф.п. – толщина фронта пламени
Узкая полоска между исходной смесью (1) и продуктами горения (ПГ) (3) и есть пламя (2). Для большинства углеводородных смесей с воздухом толщина этой полоски 0,1-1,0 мм. Это зона горения или фронт пламени. В ней протекает химическая реакция и выделяется все тепло. Свечение является результатом присутствия в ней радикалов СН, НСО, С 2 и т.д.
Таким образом, фронт пламени – это узкая светящаяся зона, разделяющая ПГ и исходную горючую смесь.
Во фронте пламени в результате химической реакции горения концентрация исходных компонентов резко снижается до нуля, а температура достигает максимального значения. Вследствие молекулярной теплопроводности температура перед зоной реакции монотонно повышается от начальной температуры горючей смеси до температуры, близкой к температуре горения, образуя зону физического прогрева.
Поскольку толщина зоны пламени не превышает, как правило, долей мм, то условно фронт пламени считают плоскостью.
Если фронт пламени движется, то пламя называют нестационарным , если не перемещается – стационарным .
Основными характеристиками являются:
Нормальная скорость распространения пламени – скорость перемещения фронта пламени относительно несгоревшего газа в направлении, перпендикулярном к его поверхности. Нормальная скорость есть функция ряда физико-химических свойств смеси и скорости химической реакции при температуре горения.
Это одна из характеристик пожарной опасности газообразных веществ. Поскольку она определяется физико-химическими свойствами горючей смеси, ее еще называют фундаментальной.
Массовая скорость выгорания. Это масса вещества, сгорающая в единицу времени с единицы площади поверхности фронта пламени.
Существуют две теории, объясняющие природу распространения пламени по горючей смеси.
Согласно диффузионной теории перемещение фронта пламени происходит за счет диффузии образующихся в зоне горения активных частиц – радикалов – в свежую смесь, где они инициируют протекание химической реакции.
Согласно тепловой теории перемещение фронта пламени осуществляется благодаря передаче тепла путем теплопроводности в свежую смесь, за счет чего последняя разогревается до температуры самовоспламенения с последующим протеканием химической реакции.
На самом деле имеют место элементы и той, и другой теорий, т.к. процесс очень сложный.
Факторы, влияющие на нормальную скорость:
Концентрация и состав горючей смеси.
Теоретически u н должна быть максимальной при j ст. Практически максимум приходится на смесь, содержащую горючего больше стехиометрического соотношения (a в < 1 – богатая смесь). u н для различных газов составляет ~ 0,3 – 1,6 м/с. Она редко превышает значение 2,5 м/с, а для углеводородно-воздушных смесей находится в пределах 0,4 – 0,8 м/с. Смеси, имеющие u н < 0,04 м/с, не способны к распространению пламени.
Присутствие флегматизаторов (N 2 , CO 2 , H 2 O (пар) , Ar и т.д.).
Наблюдается эффект разбавления, что влечет за собой снижение скорости реакции, тепловыделения и u н. Эффективность газов-флегматизаторов определяется их теплофизическими свойствами.
Температура (начальная) горючей смеси. С возрастанием Т о увеличивается температура горючей смеси: Т г = Т о + Q н /(åс р i V ПГ i)