Люминесценция. Спектры люминесценции. Виды люминесценции. Закон Стокса для фотолюминесценции. Хемилюминесценция. Люминесцентная микроскопия.
Люминесценцией называют избыточное над тепловым излучение тела, имеющее длительность, значительно превышающую период (~10 -15 с) излучаемых световых волн.
Первая часть определения отделяет люминесценцию от равновесного теплового излучения. Люминесценция обычно наблюдается в видимой или ультрафиолетовых областях спектра. Тепловое излучение в этой области возникает только при температуре в несколько сотен или тысяч градусов, тогда как люминесценция наблюдается при любых температурах, поэтому люминесценцию часто называют холодным свечение.
Признак длительности в этом определении был предложен С. И. Вавиловым для того, чтобы отличить люминесценцию от некоторых других явлений вторичного свечения, например отражения или рассеяния света.
Люминесцируют электронно-возбужденные молекулы (атомы). В зависимости от способа возбуждения различают несколько типов люминесценции.
Люминесценция, вызванная заряженными частицами: ионами – ионолюминесценция, электронами – катодолюминесценция, ядерным излучением – радиолюминесценция. Люминесценцию под воздействием рентгеновского и Y(гамма)-излучения называют рентгенолюминесценцией, фотонов видимого света – фотолюминесценция. При растирании, раздавливании или раскалывании некоторых кристаллов возникает триболюминесценция. Электрическим полем возбуждается электролюминесценция, частным случаем которой является свечение газового разряда. Люминесценцию, сопровождающую экзотермическую химическую реакцию, называют хемилюминесценцией.
Спектры Люминесценции
Спектром люминесценции называют зависимость интенсивности люминесцентного излучения от длины волны испускаемого света. Наиболее простые - атомные спектры, в которых указанная выше зависимость определяется только электронным строением атома. Спектры молекул гораздо более сложные вследствие того, что в молекуле реализуются различные деформационные и валентные колебания. При охлаждении до сверхнизких температур сплошные спектры люминесценции органических соединений, растворенных в определенном растворителе, превращаются в квазилинейчатые. Это явление получило название эффекта Шпольского. Это ведёт к снижению предела обнаружения и повышению избирательности определений, расширению числа элементов, которые можно определять люминесцентным методом анализа.
Фотолюминесценцией называется излучение электромагнитной энергии, возбуждаемое в веществе под действием оптического излучения ультрафиолетового или видимого диапазонов, избыточное по сравнению с тепловым излучением, при условии, что такое избыточное излучение имеет длительность, превышающую период электромагнитных колебаний (люминесценция) и время релаксационных процессов. Если облучить вещество (люминофор) в любом агрегатном состоянии ультрафиолетовым или видимым электромагнитным излучением, то возможно появление задержанного не менее, чем на 10-12 - 10-10 с, люминесцентного излучения. Максимум спектра этого излучения сдвинут относительно максимума спектра возбуждающего излучения в сторону меньших частот (закон Стокса - Ломмеля).
Хемилюминесценция - люминесценция (свечение) тел, вызванная химическим воздействием или при протекании химической реакции.Хемилюминесценция связана с экзотермическими химическими процессами.
Хемилюминесценция применяется для оценки состава сложных газовых смесей, в частности, наличия примесей в атмосфере. Достоинством этого метода является легкость автоматизации измерения и высокая селективность. Недостаток - ограниченный перечень анализируемых веществ.
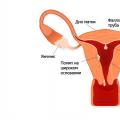
Люминесцентная микроскопия – метод микроскопии, позволяющий наблюдать первичную или вторичную люминесценцию микроорганизмов, клеток, тканей или отдельных структур, входящих в их состав.
Цвет люминесценции, т.е. длина волны излучаемого света зависит от химической структуры и от физико–химического состояния микроскопируемого объекта, что и обусловливает возможность использования л.м. в целях микробиологической и цитологической диагностики, для дифференцирования отдельных компонентов клеток.
Люминесцентный микроскоп снабжен мощным источником освещения с большой поверхностной яркостью, максимум излучения которого находится в коротковолновой области видимого спектра, системой светофильтров, а также интерференционной светоделительной пластинкой, применяемой при возбуждении люминесценции падающим светом.
Источниками освещения для люминесцентного микроскопа чаще являются ртутно-кварцевые лампы сверхвысокого давления, а также лампы накаливания: ксеноновые и кварцево-галогенные.
Для возбуждения люминесценции при люминесцентной микроскопии обычно используют длинноволновую ультрафиолетовую, сине-фиолетовую, а иногда и зелёную область спектра, в люминесцентном микроскопе применяют обычно стеклянную оптику и обычные предметные и покровные стёкла, пропускающие излучение в этой части спектра и не обладающие собственной люминесценцией. Иммерсионные и заключающие среды также должны соответствовать этим требованиям.
Основными преимуществами Люминесцентной микроскопии являются высокая чувствительность (чувствительнее обычных цито- и гистохим. методов не менее чем в 1000 раз), легкость количественного измерения содержания различных хим. компонентов ткани и клеток, доступность аппаратуры. Для Л. м. органов и тканей используют первичную и вторичную люминесценцию.
Спектрофотометрия. Спектрофлуориметрия.
Спектрофотометрия - физико-химический метод исследования растворов и твёрдых веществ, основанный на изучении спектров поглощения в ультрафиолетовой (200-400 нм), видимой (400-760 нм) и инфракрасной (>760 нм) областях спектра. Основная зависимость, изучаемая в спектрофотометрии зависимость интенсивности поглощения падающего света от длины волны. Спектрофотометрия применяется при изучении строения и состава различных соединений, для качественного и количественного определения веществ (определения следов элементов в металлах, сплавах, технических объектах). Приборы спектрофотометрии - спектрофотометры.
Спектрофлуориметрия . Принцип - испускание света, длина волны которого больше чем длина волны поглощенного света. . Применение - количественный анализ, кинетика, качественный анализ.
Лазер. Распределение Больцмана. Понятия инверсной заселённости, вынужденного излучения. Рабочее вещество лазера. Виды источников энергетической накачки. Основные компоненты конструкции лазера. Особенности лазерного излучения.
Лазер – квантовый генератор видимого диапазона излучения.
Виды рабочего вещества лазера: газовые, жидкостные, полупроводниковые и твердотельные.
Виды источников энергетической накачки: возбуждение очень интенсивным светом – « оптическая накачка», электрическим газовым разрядом, в полупроводниковых лазерах – электрическим током.
Распределение Больцмана
Распределение частиц по потенциальным энергиям в силовых полях – гравитационном, электрическом и др. – называют распределение Больцмана.
Применительно к гравитационному полю это распределение может быть записано в виде зависимости концентрации n молекул от высоты h над уровнем Земли или от потенциальной энергии молекулы m 0 gh:
Это выражение справедливо для частиц идеального газа.
Основными компонентами конструкции лазерной установки являются активная среда лазера, лазерная энергия накачки, высокий отражатель, прибор сцепки и лазерный луч. Активная среда лазера расположена в рефлексивной оптической впадине, куда направляется энергия накачки. Активная среда лазера – это материал, обладающий определенными свойствами, которые позволяют усиливать свет стимулируемой эмиссией. В своей самой простой форме эта впадина активной среды состоит из двух зеркал (одно из которых прозрачно), расположенных таким образом, что свет прыгает назад-вперед, каждый раз проходя через активную среду.
Свет, проходя через активную среду, неоднократно усиливается, выходя пучком лучей со стороны прозрачного зеркала. Энергия накачки лазера, как правило, поставляется как электрический ток или как свет волнами различной длины. Такой свет может быть обеспечен лампой или другим лазером. Большинство практических лазеров содержит дополнительные элементы, которые отвечают за такие свойства, как длина волны излучаемого света или форма луча.
Лазерное излучение уникально благодаря трем только ему присущим свойствам.
1) Когерентность. В физике существует 2 типа когерентности - пространственная и временная. Пространственная когерентность выражается в однотипности волнового фронта, т. е. пики и спады волн располагаются параллельно, когда свет выходит из лазера. Это обеспечивает синхронизацию фаз и фокусировку на очень маленькие участки.
2) Монохромность (временная когерентность). Это означает, что световые волны имеют одинаковую длину. Некоторые лазеры испускают лучи разной длины волны. Но явление это предсказуемо, и лазеры излучают свет только той длины, которая предусмотрена используемой в лазере средой.
3) Коллимация . Это означает, что все лучи, испускаемые лазером, параллельны и не рассеиваются с расстоянием.
51. Виды радиоактивных излучений. Радиоактивность. Закон радиоактивного распада. Радиоактивность-явление самопроизвольного превращения одних атомных ядер в другие, сопровождающееся испусканием различных видов ионизирующих излучений.
Основные типы радиоактивного распада:
А льфа-распад состоит в самопроизвольном превращении одно ядра в другое с испусканием α-частиц.
Пример альфа-распада для изотопа 238 U
Бета-распад заключается во внеядерном взаимном превращении нейтрона и протона.
 Закон радиоактивного распада: число радиоактивных ядер, которые ещ не распались, убывает со временем по экспоненциальному закону:
Закон радиоактивного распада: число радиоактивных ядер, которые ещ не распались, убывает со временем по экспоненциальному закону:
52.Ионизирующим излучением называется любое излучение, взаимодействие которого с веществом приводит к образованию ионов разных знаков.
Взаимодействие с веществом α– излучения
α-частицы сильно взаимодействуют с различными веществами, т. е. легко поглощаются ими. Тонкий лист бумаги или слой воздуха толщиной несколько сантиметров достаточны для того, чтобы полностью поглотить α-частицы.
При прохождении через вещество a-частицы почти полностью отдают свою энергию в результате электростатического взаимодействия с электронами оболочек атомов.
Энергия α-частиц идет на ионизацию и возбуждение атомов поглощающей среды (ионизационные потери). Этот процесс может рассматриваться как упругое столкновение α-частицы с электронами, при котором a-частица теряет часть своей энергии.
Взаимодействие с веществом β- излучения
β-частицы - это электроны (или позитроны), испускаемые ядрами радонуклидов при β-распаде.
Вероятность взаимодействия β-частиц с веществом меньше, чем для α-частиц, так как β-частицы имеют в два раза меньший заряд и приблизительно в 7300 раз меньшую массу.
Взаимодействие электронов и позитронов с веществом качественно одинаково и складывается из трех основных процессов:
упругого рассеяния на атомных ядрах;
рассеяния на орбитальных электронах;
неупругих столкновений с атомным ядром.
В случае применения тяжелых материалов возникает тормозное (вторичное) излучение , которое является рентгеновским и обладает большой проникающей способностью.
Статистика.
1.Случайное событие – это событие, которое при данных условиях может произойти, либо не произойти. Относительная частота событий называется вероятностью и показывает отношение числа ожидаемых событий к числу возможных.Статистическое определение вероятности подразумевает под собой вероятность как предел, к которому стремится относительная частота. При классическом определении отн. частота и вероятность совпадают. В этом случае должно быть известно должны быть известны полное число возможных событий и число ожидаемых событий (орёл-решка, кубики и тп).Совместные события могут происходить параллельно друг другу; несовместные события исключают появление друг друга в ходе проводимого опыта. Зависимым называется событие, на вероятность которого оказывает влияние исход какого-либо иного события. Независимые наоборот.
2.Теорема сложение вероятностей : вероятность появление какого-либо события из нескольких несовместных равна сумме их вероятностей (или то, или другое)Теорема умножения вероятностей : Вероятность совместного появления независимых событий равна произведению их вероятностей(и то и другое).Условная вероятность - вероятность одного события при условии, что другое событие уже произошло(опыт с шариками в мешке, которые вытаскивают и не возвращают)
3. Дискретные. Соотношение между возможными значениями случайной величины и их вероятностями называется законом распределения дискретной случайной величины(возможные значения которой образуют конечную или бесконечную последовательность чисел). Закон распределения может быть задан аналитически, в виде таблицы или графически. Математическое ожидание Дисперсия
4. Непрерывные случайные величины всегда имеют вероятность равную нулю, поскольку количество её возможных численных значений бесконечно велико.Математическое ожидание имеет смысл среднего значения случайной величины. Для дискретных случ. величин оно определяется как сумма произведений случ. величины на вероятность её появления. Дисперсия описывает разброс случ. величин относительно математического ожидания. Дисперсия дискретных случ. величин определяется, как сумма квадратов разности случ. величин и математического ожидания на соответствующие вероятности появления этих случайных величин.Среднее квадратичное отклонение - это квадратный корень из среднего арифметического всех квадратов разностей между данными величинами и их средним арифметическим.
5. Случайная величина называется дискретной случайной величиной , если она принимает не более чем счетное число значений. Примеры :
1) дискретная случайная величина Бернулли(закон распределения Бернулли). Закон распределения дискретной случайной величины Бернулли имеет следующий вид: 0 Такому распределению соответствует бросание монеты, на одной стороне которой - 0, а на второй - 1. 2) дискретная биномиальная случайная величина (биномиальное распределение). Закон распределения данной дискретной случайной величины запишется следующим образом: Число успехов в n испытаниях схемы Бернулли имеет биномиальное распределение. 3) дискретная случайная величина Пуассона(пуассоновское распределение с параметром). Закон распределения дискретной случайной величины Пуассона задается следующим образом: Где - параметр. Закон распределения случайной величины Пуассона носит название закона редких событий, например, число вызовов, поступивших на телефонную станцию, число распавшихся нестабильных частиц и т.д. 4) дискретная геометрическая случайная величина (геометрическое распределение). Закон распределения геометрической дискретной случайной величины имеет вид Пусть производятся независимые испытания, причем в каждом испытании возможны два исхода - "успех" с вероятностью p или "неуспех" с вероятностью 1 - p , 0 < p < 1 . Обозначим через число испытаний до первого появления "успеха", тогда будет дискретной геометрической случайной величиной. Распределение случайной величины называется непрерывным
, а сама случайная величина - непрерывной случайной величиной, если для любого Примеры
1) нормальная непрерывная случайная величина, или непрерывная случайная величина Гаусса(нормальное распределение).Важная роль этого распределения объясняется тем, что оно обычно возникает в явлениях, подверженных действию большого числа малых случайных величин. Так, математическая теория выборочного метода в статистике для расчета некоторых показателей широко использует нормальное распределение. 2)экспоненциальная (показательная) непрерывная случайная величина(экспоненциальное распределение).Экспоненциальному распределению подчиняется время распада ядер атомов различных элементов. Оно обладает важным свойством - отсутствием последствия. Несложно убедиться в том, что вероятность распада ядра за время при условии, что перед этим оно уже прожило время, совпадает с безусловной вероятностью распада того же самого ядра за время. Именно это свойство и представляет собой отсутствие последствия. 3) Равномерная на непрерывная случайная величина(равномерное на отрезке распределение).Равномерное распределение реализует принцип геометрической вероятности при бросании точки на отрезок . Закон Бернулли
: число ожидаемых событий, появляющихся в опытах с n независимыми испытаниями, в которых ожидаемые события характеризуются одинаковой вероятностью p или: Математическое ожидание Пусть - случайная величина, определённая на некотором вероятностном пространстве. Тогда где символ M обозначает математическое ожидание. 6. смотри билет 5 Закон распределения Пуассона:
удовлетворяет вероятности появления заданного количества редко происходящих случайных событий, наблюдаемых в серии из большого количества независимых повторных опытов. Вероятность намного меньше 1. Где m-число ожидаемых событий, а- параметр распределения, совпадающий с математическим ожиданием, е-основание натурального логарифма. Распределению Пуассона удовлетворяют числа редких событий, происходящих за определённый промежуток времени. 7. Непрерывные и дискретные случайные величины. Плотность вероятности. Нормальный закон распределения. Математическое ожидание и дисперсия. Графическое представление. Примеры
. Дискретные случайные величины – величины, которые могут принимать счетное количество значений конечное или бесконечное. Непрерывные случайные величины- величины. Которые принимают бесконечное число возможных значений в конечном, или в бесконечном интервалах изменения Плотностью вероятности f(x) непрерывной случайной величины Х называется производная функции распределения F(X) этой величины: f(x)=F’(X) Основные свойства плотности: 3).определенный интеграл в пределах от минус бесконечности до плюс бесконечности от плоности вероятности непрерывной случайной величины равен единице.. 4)определенный интеграл в пределах от «–« бесконечности до х от плотности вероятности непрерывной случайной величины равен функции распределения этой величины. где параметр μ
σ
² - дисперсия. 8. Стандартное нормальное распределение. Стандартные интервалы. Понятия доверительного интервала и доверительной вероятности
. Доверительный интервал - это интервал, построенный с помощью случайной выборки из распределения с неизвестным параметром, такой, что он содержит данный параметр с заданной вероятностью. Пусть - выборка из некоторого распределения с плотностью , зависящей от параметра , который может изменяться в интервале . Пусть - некоторая статистика и - функция распределения случайной величины выполняются с вероятностью , близкой к единице. Перепишем неравенства (1) в другом виде: (2) Обозначим , и запишем (2) в следующем виде: Интервал называется доверительным интервалом для параметра
, а вероятность - доверительной вероятностью
. Нормальное распределение, также называемое распределением Гаусса - распределение вероятностей, которое задается функцией плотности распределения: где параметр μ
- среднее значение (математическое ожидание) случайной величины и указывает координату максимума кривой плотности распределения, а σ
² - дисперсия. Графики нормального распределения 9.
Понятие генеральной совокупности и выборки. Объём выборки, репрезентативость. Статистическое распределение (вариационный ряд). Примеры. Характеристики выборки.
Генеральная совокупность – множество каких-либо однородных элементов, которые предстоит изучить статистическими методами; множество всех значений случайной величины, а варианта – одно из значений генеральной совокупности. Выборка – это некоторая часть элементов, выделяемая по определенному правилу из ген. совокупности. Объём выборки – это число выделяемых элементов в генеральной совокупности. Минимальным, статистическим допустимым объёмом выборки, считается три элемента. Выборка производится с целью описания генеральной совокупности. Если это описание является полным и корректным, то выборка является репрезентативной. Результаты повторных измерений какой-либо физической величины х, проводимых в одинаковых условиях, часто называют выборкой из бесконечной генеральной совокупности, поскольку считается, что в опыте теоретически возможно произвести сколь угодно большое число измерений при одинаковых условиях, а множество всех возможных результатов измерений и образуют данную генеральную совокупность. Математическое ожидание такой генеральной совокупности считается истинным значением измеряемой величины.Таким образом, в ходе нескольких повторных измерений физической величины получают набор результатов, являющийся выборкой объёма n:х 1 , х 2 ,…..,х n , где n-число повторных измерений.Как дискретные, так и непрерывные, случайные величины могут быть получены в результате опыта – наблюдения – то есть в виде вариационнго ряда: 4,67; 5,49; 5351 и так далее. Однако такой способ задания является малоинформативным – требующим дополнительной обработки, для какого-либо даже поверхностного представления о случайной величине. К выборочным характеристикам отнтсятся: · среднее значение (Х ср), как оценка математического ожидания · выборочное среднеквадратическое отклонение (S x), как оценка генерального значения среднеквадратического отклонения (σ) выборочная дисперсия (S x 2) N- число элементов выборки № 10 Точечные оценки параметров генеральной совокупности.
Пусть выборка объема n
представлена в виде вариационного ряда. Назовем выборочной средней
величину Величина называется относительной частотой
значения признака x i
. Если значения признака, полученные из выборки не группировать и не представлять в виде вариационного ряда, то для вычисления выборочной средней нужно пользоваться формулой . Выборочную дисперсию Приведем еще один пример точечной оценки. Пусть каждый объект генеральной совокупности характеризуется двумя количественными признаками x
и y
. Например, деталь может иметь два размера – длину и ширину. Можно в различных районах измерять концентрацию вредных веществ в воздухе и фиксировать количество легочных заболеваний населения в месяц. Можно через равные промежутки времени сопоставлять доходность акций данной корпорации с каким-либо индексом, характеризующим среднюю доходность всего рынка акций. В этом случае генеральная совокупность представляет собой двумерную случайную величину x,h.
Эта случайная величина принимает значения x
, y
на множестве объектов генеральной совокупности. Не зная закона совместного распределения случайных величин x иh, мы не можем говорить о наличии или глубине корреляционной связи между ними, однако некоторые выводы можно сделать, используя выборочный метод. Выборку объема n
в этом случае представим в виде таблицы, где Выборочный коэффициент корреляции рассчитывается по формуле Выборочный коэффициент корреляции можно рассматривать как точечную оценку коэффициента корреляции r x h , характеризующего генеральную совокупность. Выборочные параметры или любые другие зависят от того, какие объекты генеральной совокупности попали в выборку и различаются от выборки к выборке. Поэтому они сами являются случайными величинами. Пусть выборочный параметр dрассматривается как выборочная оценка параметра D генеральной совокупности и при этом выполняется равенство M
d =
D.
Такая выборочная оценка называется несмещенной.
Для доказательства несмещённости некоторых точечных оценок будем рассматривать выборку объема n
как систему n
независимых случайных величин x 1 ,x 2 ,... x n
, каждая из которых имеет тот же закон распределения с теми же параметрами, что и случайная величина x
, представляющая генеральную совокупность. При таком подходе становятся очевидными равенства: Mx i
= M
x i
=M
x; Интервальные оценки.
Точечные оценки параметров генеральной совокупности могут быть приняты в качестве ориентировочных, первоначальных результатов обработки выборочных данных. Их недостаток заключается в том, что неизвестно, с какой точностью оценивается параметр. Если для выборок большого объема точность обычно бывает достаточной (при условии несмещенности, эффективности и состоятельности оценок), то для выборок небольшого объема вопрос точности оценок становится очень важным. Введем понятие интервальной оценки неизвестного параметра генеральной совокупности (или случайной величины x
, определенной на множестве объектов этой генеральной совокупности). Обозначим этот параметр черезD
. По сделанной выборке по определенным правилам найдем числа D
1 и D
2 , так чтобы выполнялось условие: P
(D
1 <D
<D
2) =P
(D
Î(D
1 ; D
2)) = g Числа D
1 и D
2 называются доверительными границами
, интервал (D
1 , D
2) - доверительным интервалом
для параметра D
. Число g называется доверительной вероятностью
или надежностью
сделанной оценки. Сначала задается надежность. Обычно ее выбирают равной 0,95, 0,99 или 0,999. Тогда вероятность того, что интересующий нас параметр попал в интервал (D
1 , D
2) достаточно высока. Число (D
1 + D
2) / 2 – середина доверительного интервала – будет давать значение параметра D
с точностью
(D
2 – D
1) / 2, которая представляет собой половину длины доверительного интервала. Границы D
1 и D
2 определяются из выборочных данных и являются функциями от случайных величин x
1 , x
2 ,...,x n
, а следовательно – сами случайные величины. Отсюда – доверительный интервал (D
1 , D
2) тоже случаен. Он может покрывать параметр D
или нет. Именно в таком смысле нужно понимать случайное событие, заключающееся в том, что доверительный интервал покрывает число D.
11. Графические характеристики случайных величин. Гистограмма. Характеристики положения (мода, медиана, выборочная средняя).
Фотопроцессы в биологических системах сопровождаются возникновением электронно-возбужденных состояний, характеризующихся определенной энергией, временем жизни, структурными свойствами. Полная энергия состояния молекулы Е складывается из энергии электронного возбуждения Ее, колебательной энергии Еv и вращательной энергии Er. Таким образом, при поглощении кванта света молекулой полное изменение энергии можно представить в следующем виде: ашню = дельта Ее + дельта Еv + дельта Er . Энергия вращательных квантов меньше, чем колебательных, а их энергия, в свою очередь, меньше энергии электронных (Er 10 в10 Гц, Еv 10 в 13 Гц, Ее 10 в 18 Гц). Возможные электронные переходы и энергетические состояния молекулы обычно представляются в виде схемы уровней энергии (Яблонского), где каждый электронный уровень расщепляется на ряд колебательных подуровней, а каждый колебательный - на ряд вращательных подуровней (рис. 1) При поглощении кванта света молекулой осуществляется переход с самого нижнего колебательного подуровня основного состояния (комнатная температура) на возбужденные уровни S1* и S2*, характеризующиеся колебательными и вращательными подуровнями. В молекулах большинства соединений при возбуждении электронных состояний, расположенных выше S1*, происходит быстрая внутренняя конверсия (с временами порядка 10 в -13 с) за счет перехода с нижнего колебательного подуровня верхнего состояния S2* на верхний колебательный подуровень нижнего состояния S1* с последующей релаксацией (порядок 10 в -12) на самый нижний колебательный подуровень возбужденного состояния S1*. Это означает, что в какое бы возбужденное состояние ни попала молекула (например, в состояние S2*), в течение 10 в -13 - 10 в -12 с она перейдет на нижний колебательный подуровень первого электронного состояния S1*. Именно с этого уровня при переходе на любой колебательно-вращательный подуровень основного состояния S0 и происходит излучение - флуоресценция. Отсюда следует, что спектр флуоресценции I=f(лямбда), т.е. зависимость интенсивности флуоресценции от длины волны и квантовый выход флуоресценции фи=число квантов фл/число погл квантов не зависят от длины волны возбуждающего света. Независимость спектра и квантового выхода флуоресценции от энергии поглощенного молекулой кванта называется законом Вавилова. Поскольку энергия поглощенного кванта частично растрачивается на тепловые колебания, энергия кванта флуоресценции оказывается меньшей, т. е. спектр флуоресценции сдвинут в длинноволновую сторону относительно наиболее длинноволновой полосы поглощения (закон Стокса) (т.к. E=hc/лямбда, чем меньше энергия, тем длиннее лямбда). Если что рисуем 2 гладких холма, где правый – спектр флуоресценции, а левый – поглощения. Форма полос флуоресценции определяется распределением колебательных подуровней основного состояния, т. е. отражает колебательную структуру основного состояния S0. Часто распределение колебательных подуровней по энергиям у основного и возбужденного состояний одинаково; следовательно, полосы флуоресценции и поглощения будут зеркально симметричны относительно так называемого (0 - 0)-перехода (единственный переход, имеющий одинаковую энергию поглощения и флуоресценции). Принцип Франка – Кондона: электронные переходы в молекулах происходят очень быстро (около 10 в -15 с) по сравнению с движением ядер, благодаря чему расстояние между ядрами и их скорости при электронном переходе не успевают измениться. Существует несколько дополнительных формулировок этого принципа: электроны не обмениваются энергией с ядрами; электроны всегда имеют равновесную конфигурацию при любом расположении ядер. Зависимость потенциальной энергии системы от координат ядер многоатомной молекулы в основном и возбужденном состояниях различается. В наиболее простом случае (двухатомная молекула) минимумы кривых потенциальных энергий в основном и возбужденном состояниях сдвинуты, поскольку орбиталь, заполняемая электроном в возбужденном состоянии, занимает большую область пространства, чем в основном состоянии, и положение равновесия в возбужденном состоянии, следовательно, соответствует большему межъядерному расстоянию (поэтому сдвиг). Кроме того, форма таких потенциальных кривых в основном и возбужденном состояниях также различается (рис. 2). В соответствии с принципом Франка - Кондона наиболее вероятным будет такой переход, при котором не произойдет изменений ни в положении ядер, ни в импульсе (принцип вертикальности перехода между двумя электронными состояниями). Решение волнового уравнения показывает, что хотя при поглощении кванта света возможны различные переходы, однако наиболее вероятным будет переход, обозначенный сплошной стрелкой вверх на рис. 2. Иными словами, наиболее вероятное межъядерное расстояние для молекулы с нулевой колебательной энергией соответствует середине АВ. В случае флуоресценции наиболее вероятным будет испускание из середины CD (сплошная стрелка вниз), что соответствует наиболее интенсивной полосе спектра. Флуоресценция происходит с самого нижнего колебательного уровня первого возбужденного состояния при переходе молекулы в основное состояние. Вероятность перехода из возбужденного в основное состояние может быть описана константой скорости перехода k, которая по физическому смыслу эквивалентна константе мономолекулярной реакции. Кинетика перехода может быть описана реакцией первого порядка dS*/dt=-kS*, где S* - количество возбужденных молекул. После интегрирования волшебным образом I=Io*exp(-kt), k – константа флуоресценции. При отсутствии безызлучательных процессов (фи= 1) длительность пребывания молекулы в возбужденном состоянии определяется радиационным, или естественным, временем жизни тау0=1/константу флуоресценции. Это то время, в течение которого число возбужденных молекул уменьшается в e раз. В реальных ситуациях квантовый выход обычно меньше единицы, поскольку с флуоресценцией конкурируют безызлучательные процессы: интеркомбинационная конверсия с переходом в триплетное возбужденное состояние, сопровождающееся изменением спина, внутренняя конверсия, диссипация в тепло, фотохимическая реакция или дезактивация за счет тушения флуоресценции при взаимодействии с молекулами тушителя Q. В действительности квантовый выход флуоресценции меньше единицы вследствие существования в молекуле безызлучательных процессов; следовательно, реальное (или измеряемое) время жизни тау флуоресц окажется меньше тау): 1/сумму констант происходящих процессов (флуоресценция, фотосинтез, интеркомбинационная конверсия в триплетное состояние, диссипация в тепло (внутренняя конверсия), тушение*[Q]). Квантовый выход флуоресценции в этом случае выражается соотношением: фи=константа флуоресценции/сумму констант происходящих процессов, т.е. Фи=константа флуоресценции*время жизни. В отсутствие тушителя квантовый выход флуоресценции обозначают как фи фл0. Фи фл0/фи фл= 1 + константаq*[Q])/сумму всех констант без тушителя, то, обозначив время жизни в отсутствие тушителя через тау фл0 (не путать с тау0 которая вообще без побочных процессов), получим, что тау фл0 =1/ сумму всех констант без тушителя и (фи фл0/фи фл)–
1=
тау фл0* константаq*[Q]=K[Q]. I=I0/(1+ K[Q]). Последнее уравнение называется соотношением Штерна и Фольмера, а К - константой тушения. Последняя легко определяется экспериментально при измерении интенсивностей флуоресценции различных образцов, отличающихся концентрацией тушителя. Для этого достаточно оценить угловой коэффициент прямой в координатах I без тушителя/(Iс тушителем - 1) и [Q]. Исходя из определения квантового выхода флуоресценции фи=I фл/(I0-Iпрошедшего через объект), с использованием закона Ламберта - Бэра можно установить связь между интенсивностью флуоресценции I и молярным коэффициентом поглощения, а также концентрацией с: I=K*I0*(1-Т)*фи, где I0- интенсивность возбуждающего света, (1 - Т) - величина поглощения, Т - величина пропускания, К - коэффициент пропорциональности, зависящий от способа измерения. Так как D= - lg Т = эпсилон*с1, где D - оптическая плотность, то I=K*I0*(1-10 в степени -D)*фи. Выражение в скобках можно разложить в ряд при небольших значениях D и ограничиться линейным членом: I примерно=2,3K*I0*эпсилон*cl*фи Это означает, что при малых оптических плотностях (меньше 0,1-0,2) I пропорциональна концентрации флуоресцирующего вещества и интенсивности возбуждающего света. Точное измерение интенсивности флуоресценции осложняется целым рядом факторов: реабсорбцией флуоресценции, экранированием возбуждающего света другими молекулами, светорассеянием, гетерогенностью объекта, миграцией энергии, тушением флуоресценции. При комнатной температуре квантовый выход флуоресценции хлорофилла в нативных фотосинтетических мембранах составляет не более 3%. Низкотемпературная техника может ослабить влияние возбуждающего света, вызывающего побочные процессы. Флуоресценция хлорофилла в нативных фотосинтетических мембранах продуцируется молекулами хлорофилла антенны и при комнатной температуре характеризуется главным максимумом 684-687 нм и «плечом» в более длинноволновой области около 720-730 нм. В случае целых листьев из-за реабсорбции доля длинноволновой полосы возрастает. При комнатной температуре квантовый выход для фотосистемы 1 в несколько раз меньше, чем для фотосистемы 2. Люминесценция - «холодное» свечение некоторых веществ (люминофоров); излучение, представляющее собой избыток над тепловым излучением тела при данной температуре и имеющее длительность, значительно превышающую период световых волн. Характеристики: спектр возбуждения, спектр люминесценции, квантовый выход, время жизни молекулы в возбужденном состоянии. Она делится на уже описанную флуоресценцию (быструю люмин) и фосфоресценцию (медленную люмин). Фосфоресценция – переход с нижнего колебательного уровня триплетного состояния T1 на основное возбужденное (время жизни возбужденного состояния при фосфоресценции составляет порядка 10 в −2 – 10 в −4 с, т.к. синглет-триплетные переходы имеют квантово-механический запрет – так может делать хлорофилл). Механизмы миграции хорошо отражает рис 3 и описанные ранее процессы. Рис. 3. Схематическое изображение физического механизма люминесценции: жирными горизонтальными линиями обозначены энергетические состояния молекулы люминесцирующего вещества; S0 - основное (невозбужденное) состояние; S2, S2 и Т1 - возбужденные состояния; тонкими горизонтальными линиями обозначены колебательные уровни (0, 1, 2.,. или 0’, 1’, 2’ и т.д.); в прямоугольниках показано направление спина возбужденного электрона (слева) по отношению к спину оставшегося электрона; ВК - внутренняя конверсия (переходы электрона без обращения спина); ИК - интеркомбинационная конверсия (переходы электрона с обращением спина). При поглощении энергии молекула переходит в возбужденное состояние S1 или S2 (обозначено синими вертикальными стрелками). Часть поглощенной энергии преобразуется в тепло (обозначено волнистыми стрелками), при этом молекула переходит на нижний колебательный уровень состояния S1 или трансформируется в состояние Т1 Возвращение молекулы из состояния S1 или Т1 на исходный энергетический уровень может сопровождаться излучением света - флюоресценцией (обозначена темно-зелеными стрелками) или фосфоресценцией (обозначена светло-зелеными стрелками). Люминесценция биологических объектов может быть собственной (первичной) либо возникать после соответствующей химической модификации имеющихся веществ (вторичная), а также после введения так называемых флюоресцентных зондов. Флюоресцирующие соединения могут быть определены в очень низких концентрациях, часто в присутствии посторонних веществ. Поэтому регистрация люминесценции успешно используется для количественного определения многих биологически важных веществ. Одним из наиболее ярко флюоресцирующих лекарственных соединений является хинин. В кислых растворах он люминесцирует в синей области (450-475 нм). Чтобы определить его в плазме крови проводят осаждение белков метафосфорной кислотой и измеряют люминесценцию хинина прямо в фильтрате. Яркой синей флюоресценцией обладает противогрибковый препарат гризеофульвин, он легко определяется в экстрактах из крови или мочи. Барбитураты в щелочной среде обладают яркой зеленой флюоресценцией, их можно определить в экстрактах из биологического материала. После экстракции возможна количественная регистрация многих витаминов, например витамина Е, максимум флюоресценции которого лежит в УФ-области при 330 нм. Витамин В6 имеет синюю, а витамин А - зеленую флюоресценцию. Витамины С, D, В12 и др. удается определить по вторичной люминесценции. Наркотические вещества морфин и героин флюоресцируют очень слабо, но после обработки образцов серной кислотой с последующим выщелачиванием возникает специфическая интенсивная синяя флюоресценция продуктов реакции. Этим методом удается определить до 0,02 мкг наркотика в пробе. Чувствительным лабораторным методом определения АТФ является регистрация хемилюминесценции в присутствии люциферина и люциферазы светлячка. Люцифераза катализирует реакцию восстановленного люциферина с АТФ; продукт этой реакции - аденилат при окислении испускает свет. По собственной люминесценции проводят контроль качества пищевых продуктов. Так, при длительном хранении молока и сливок рибофлавин окисляется в люмихром, что сопровождается изменением цвета флюоресценции от желто-зеленого к синему. Яйца, зараженные некоторыми видами бактерий рода Pseudomonas, при УФ-облучении начинают интенсивно флюоресцировать (за счет пигмента пиовердина, синтезированного этими бактериями). Регистрация люминесценции позволяет получать важную информацию о физико-химических свойствах биологических объектов в норме и патологии. Молекулярные механизмы работы цепи переноса электронов в митохондриях, целых клетках и даже в тканях изучают по изменению синей (440 нм) флюоресценции восстановленных пиридиннуклеотидов, возбуждаемой при 365 нм. При изучении структуры нуклеиновых кислот применяют акридиновый оранжевый и другие зонды. При этом определение положения максимума люминесценции в спектре позволяет судить о структуре нуклеиновой кислоты. Так, максимум акридинового оранжевого и двуспиральной нативной ДНК располагается в зеленой области спектра (530 нм), тогда как в одноцепочечной ДНК и РНК он смещается в красную область (640 нм). Микрофлюориметрически с помощью зондов анализируют ДНК непосредственно в клетках. В медицинской технике распространение получили неорганические люминофоры - вещества, способные к фото-, рентгенофлюоресценции и т.д. Биолюминесценция – видимое свечение организмов, связанное с процессами их жизнедеятельности; являет собой результат биохимической реакции, в которой химическая энергия возбуждает специфическую молекулу, и та излучает свет. Наблюдается у нескольких десятков видов бактерий, низших растений (грибов), у некоторых беспозвоночных животных (от простейших до насекомых включительно), у рыб. Светящиеся организмы иногда размножаются в таком количестве, что вызывают свечение моря. У многих организмов (бактерии, простейшие, ракообразные, грибы и др.) свечение происходит постоянно и непрерывно, если в окружающей среде есть кислород. У других биолюминесценция происходит отдельными вспышками и связана с условиями жизнедеятельности (голод, период размножения и др.). Биологическое значение биолюминесценции различно. Так, у светящихся насекомых вспышки биолюминесценции служат сигналом, позволяющим самцам и самкам находить друг друга; у ряда глубоководных рыб - для освещения и приманки добычи; у каракатицы - для защиты от хищников (путём выбрасывания светящейся жидкости) и др. В некоторых случаях источником биолюминесценции животного являются светящиеся бактерии-симбионты (например, т. н. несамостоятельное свечение ряда рыб). 1. Люминесценция, виды люминесценции. 2. Механизмы фотолюминесценции. 3. Cпектры возбуждения и люминесценции. Правило Стокса. 4. Хемилюминесценция. 5. Использование люминесценции в биологии и медицине. 6. Основные понятия и формулы. 29.1. Люминесценция, виды люминесценции
Люминесценцией
называют
свечение тел, которое не может быть объяснено их тепловым излучением.
Так, например, в видимой области спектра тепловое излучение становится
заметным только при температуре ~10 3 -10 4 К, а люминесцировать тело может при любой температуре. Поэтому люминесценцию часто называют холодным свечением.
Одной
из причин, вызывающих люминесценцию, является внешнее излучение,
которое возбуждает молекулы тела. Например, падающий свет. После
прекращения процесса облучения люминесцентное свечение не прекращается
тотчас же, а продолжается еще некоторое время. Это последействие
отличает люминесценцию от таких явлений, как отражение и рассеяние
света. В настоящее время в физике принято следующее определение
люминесценции. Люминесценция -
излучение,
представляющее собой избыток над тепловым излучением тела и
продолжающееся в течение времени, значительно превышающего период
световых колебаний (10 15 с).
Вещества, способные превращать поглощаемую ими энергию в люминесцентное свечение, называют люминофорами.
Люминесценция
- результат квантовых переходов в возбужденных атомах, молекулах,
кристаллах. По виду возбуждения различают следующие типы люминесценции: фотолюминесценция
- возникает при возбуждении атомов светом (ультрафиолетовые лучи и коротковолновая часть видимого света); рентгенолюминесценция
- возникает при возбуждении атомов рентгеновским и γ
-излучением (экраны рентгеновских аппаратов, индикаторы радиации); катодолюминесценция
- возникает при возбуждении атомов электронами (кинескопы, экраны осциллографов, мониторов); радиолюминесценция
- возникает при возбуждении атомов продуктами радиоактивного распада; электролюминесценция
-
возникает при возбуждении атомов под действием электрического поля
(возбуждение молекул газа электрическим разрядом - газоразрядные лампы); хемилюминесценция
- возникает при возбуждении молекул в процессе химических реакций; биолюминесценция
- возникает в биологических объектах в результате определенных биохимических реакций; сонолюминесценция
- возникает под действием ультразвука. Как
уже отмечалось выше, люминесценция продолжается и после прекращения
внешнего возбуждения люминофора. По длительности остаточного свечения
различают флуоресценцию
и фосфоресценцию:
флуоресценция
- кратковременное остаточное свечение, длительность которого составляет 10 -9 -10 -8 с; фосфоресценция
- продолжительное остаточное свечение, длительность которого составляет 10 -4 -10 4 с. 29.2. Механизмы фотолюминесценции
Фотолюминесценция начинается с возбуждения атома или молекулы фотоном внешнего излучения с некоторой частотой ν.
В
результате атом переходит с основного энергетического уровня (1) на
один из возбужденных уровней (2). Далее возможны три продолжения. 1. Атом (молекула) возвращается на основной уровень с испусканием фотона, частота которого равна частоте поглощенного фотона: v л
= ν
(рис. 29.1, а). Такая люминесценция называется резонансной.
Рис. 29.1.
Виды люминесценции: резонансная (а),
стоксова (б) и антистоксова (в) 2. Возбужденный
атом взаимодействует с окружающими его атомами и безызлучательно
переходит на нижний возбужденный уровень (2). Затем он переходит на
основной уровень, испуская фотон меньшей частоты: ν л
< ν
(рис. 29.1, б). Такая люминесценция называется стоксовой
(в честь Дж. Г. Стокса). 3. Возбужденный
атом взаимодействует с окружающими его атомами и переходит на верхний
возбужденный уровень Затем он переходит на основной уровень, испуская
фотон большей частоты: ν л
> ν
(рис. 29.1, в). Такая люминесценция называется антистоксовой.
29.3. Спектры возбуждения и люминесценции. Правило Стокса
В
процессе фотолюминесценции происходит преобразование поглощаемой
световой энергии в энергию люминесцентного излучения. Поглощающая
способность вещества характеризуется спектром поглощения (см. лекцию
28). Волны, при поглощении которых возникает люминесценция, образуют полосу возбуждения
(рис. 29.2). Таких полос может быть несколько. Совокупность всех полос возбуждения образует спектр возбуждения.
Распределение интенсивности люминесцентного излучения по длинам испускаемых волн называется спектром люминесценции:
I л = f(λ л).
Исследования
показали, что спектр люминесценции не меняется при изменении длины
волны возбуждающего света в пределах полосы возбуждения. Каждый люминофор характеризуется своими, только ему присущими спектрами люминесценции и поглощения. На люминесцентное излучение тратится только часть
энергии поглощаемого света. Поэтому для люминесценции выполняется правило (закон) Стокса:
Спектр люминесценции сдвинут в длинноволновую область относительно спектра поглощения того же соединения.
Правило
Стокса используется в осветительной технике для преобразования
ультрафиолетового излучения в видимый свет. Примером является ртутная
лампа, в которой пары ртути, возбуждаемые электрическим разрядом,
излучают ультрафиолет. На внутреннюю поверхность лампы нанесен слой
люминофора с подходящим спектром люминесценции в видимой области.
По сравнению с лампами накаливания такие лампы более экономичны. 29.4. Хемилюминесценция
Люминесценция, возникающая в химических реакциях, при которых происходит выделение энергии, называется хемилюминесценцией.
При этом происходит превращение химической энергии в световую. При
хемилюминесценции свет испускается либо непосредственно продуктами
реакции, либо другими компонентами, которым передается возбуждение.
Яркость хемилюминесценции пропорциональна скорости реакции. Хемилюминесценция, которая возникает в биологических объектах, называется биохемилюминесценцией.
Биохемилюминесценция присуща самым разнообразным видам живых существ (всего около 250 видов). Механизм
биохемилюминесценции определяется реакциями окисления. Например, если
поместить кусок светящейся гнилушки под колпак воздушного насоса и
откачать воздух, то свечение прекратится. Если после этого под колпак
подать воздух, то свечение возобновится. Было показано, что в
биологических системах хемилюминесценция возникает при рекомбинации
перекисных свободных радикалов липидов. Свечение при
биохемилюминесценции бывает весьма интенсивным - известен случай, когда
хирурги оперировали в полевых условиях по ночам при свете банок,
наполненных тропическими светляками. 29.5. Использование люминесценции в биологии и медицине
Люминесцентный, качественный и количественный анализы
Люминесцентный анализ -
совокупность методов для определения природы и состава вещества по спектру его люминесценции.
Качественный анализ
-
определение наличия (или отсутствия) каких-либо веществ (молекул) по
форме спектра люминесценции. При этом можно изучать структуру молекул
вещества; межмолекулярное взаимодействие; химические превращения.
Количественный анализ
- определение количества вещества по интенсивности спектра люминесценции (можно обнаружить массу вещества m = 10 -10 г). Если люминофором
является растворенное вещество, то при невысокой оптической плотности
раствора интенсивность люминесценции пропорциональна концентрации
раствора. Поэтому по интенсивности люминесценции можно судить о
концентрации раствора. Для этого интенсивность люминесценции
исследуемого раствора (Ι χ) сравнивают с интенсивностью люминесценции раствора (I 0), концентрация которого известна. Неизвестную концентрацию С х находят по формуле Проверка качества и сортировка пищевых продуктов. Сортировка фармакологических средств. Свечение волос, чешуек, ногтей при диагностике их поражения грибком и лишаем. Микроанализ
- исследование люминесцирующих микрообъектов при помощи специальных люминесцентных микроскопов,
в которых есть специальный осветитель, содержащий ртутную лампу со светофильтром, пропускающим УФ-излучение. Флуоресцентные зонды
В
некоторых медицинских исследованиях применяются специальные люминофоры,
вводимые в организм и распределяющиеся по тканям в соответствии со
своими свойствами. Такие люминофоры получили название флуоресцентных зондов.
Например,
при введении раствора такого люминофора в кровь он разносится по всему
организму и диффундирует в дерму и эпидермис. Люминесценция возбуждается
длинноволновым ультрафиолетовым излучением и наблюдается в видимом
свете. В поверхностных тканях с пониженным кровоснабжением люминесценция
появляется позже, чем в тканях с нормальным кровоснабжением. Флуоресцентные метки
Флуоресцирующие
молекулы можно ковалентно связывать с определенными молекулами, и затем
эту систему вводить в исследуемый объект. Такие молекулы называются флуоресцентными метками.
Примером
является использование флуоресцентно меченых антител. Если добавить
такие антитела к суспензии смеси клеток, то они связываются только с
теми из них, на поверхности которых Люминесценция: основные понятия ■ Упоминание о люминесценции датируется XV веком, когда было описано свечение неорганических кристаллов. Возникновение люминесценции многие связывают с моментом выхода работы Давида Брустера, который в 1833 году описал красную флуоресценцию хлорофилла. ■ The Hound of the Baskervilles (Конан Дойл Артур). Src="https://present5.com/presentation/37574361_76674408/image-5.jpg" alt="Классификация видов люминесценции n По длительности свечения: флуоресценция (~10 -8 c), фосфоресценция (>10 -6">
Классификация видов люминесценции n По длительности свечения: флуоресценция (~10 -8 c), фосфоресценция (>10 -6 с). n По способу возбуждения (таблица). n По механизму свечения: свечение дискретных центров – поглощающими и излучающими центрами являются одни и те же частицы (атомы, молекулы, ионы); рекомбинационное свечение – процессы поглощения и излучения разделены во времени и в пространстве. В процессе возбуждения происходит разделение частицы вещества на две противоположно заряженные части. Последующая их рекомбинация сопровождается выделением энергии. Понятие “люминесценция” включает в себя множество различных явлений. Существует несколько систем их классификации. В аналитической химии чаще всего используется молекулярная фотолюминесценция. В зависимости от природы основного и возбуждённого состояния молекулы её подразделяют на флуоресценцию и фосфоресценцию. Основные характеристики и закономерности люминесценции
Основными характеристиками люминесценции являются: · спектр возбуждения
, · спектр испускания
(спектр люминесценции), · квантовый и энергетический выходы
, · поляризация
, время жизни
и т.д. Спектр возбуждения люминесценции
(флуоресценции, фосфоресценции) - зависимость интенсивности испускаемого света с фиксированной длиной волны от длины волны или другой волновой характеристики возбуждающего света
. Возбуждая молекулу вещества светом с длиной волны, соответствующей l max спектра возбуждения, можно получить флуоресценцию с максимальной интенсивностью. В разбавленных растворах спектр возбуждения флуоресценции совпадает со спектром поглощения вещества. Спектр люминесценции
- зависимость интенсивности испускаемого света от его длины волны при фиксированной длине волны возбуждающего света
. В табл. 21.1 приведены основные свойства, присущие спектрам люминесценции. Основные свойства спектров люминесценции
Квантовый выход
(обозначение В кв, Q, f) - отношение числа испускаемых фотонов к числу поглощаемых
Энергетический выход
(В эн) - отношение энергии излучаемого света к энергии поглощаемого
Между В кв и В эн существует следующая взаимосвязь Поскольку обычно n исп < n погл, то В эн < В кв Квантовый выход люминесценции не зависит от l возб вплоть до некоторой l, находящейся в области наложения спектров поглощения и испускания, после чего резко уменьшается.Энергетический выход зависит от l возб: вначале он увеличивается прямо пропорционально l возб, затем на некотором интервале не изменяет своей величины, после чего резко уменьшается (закон Вавилова
). Влияние различных факторов на интенсивность флуоресценции растворов
Люминесценция и, в частности, флуоресценция в гораздо большей степени подвержена влиянию различных факторов, чем поглощение света. Интенсивность флуоресценции зависит от: · природы вещества
; · концентрации вещества в растворе
; · условий, в которых находится флуоресцирующее вещество
(температура, растворитель, рН, наличие в растворе других веществ, способных влиять на флуоресценцию). Природа вещества
Неорганические соединения (за исключением некоторых соединений урана, лантанидов) обычно не способны флуоресцировать в растворе. В то же время среди органических соединений флуоресцирующих веществ достаточно много. Необходимым
(но не достаточным!) условием для фотолюминесценции является способность вещества поглощать электромагнитное излучение УФ- или видимого диапазона
. Обычно вещества, обладающие интенсивной флуоресценцией, имеют длинную систему сопряжённых связей. Наиболее часто флуоресцирующие вещества встречаются среди ароматических соединений. Введение в бензольное кольцо электронодонорных заместителей увеличивает способность вещества флуоресцировать
. Например, многие фенолы и ароматические амины обладают интенсивной флуоресценцией. Введение электроноакцепторных заместителей
, за некоторым исключением, уменьшает флуоресценцию
. Атомы тяжёлых галогенов
(Br, I) увеличивают скорость интеркомбинационной конверсии и, тем самым, уменьшают квантовый выход флуоресценции
. Однако введение тяжёлых галогенов увеличивает способность вещества фосфоресцировать. Способность вещества к флуоресценции в растворе увеличивается при конденсации ароматических колец и увеличении «жёсткости» молекулы
. Например Концентрация вещества
Зависимость между интенсивностью флуоресценции и концентрацией флуоресцирующего вещества в растворе более сложная, чем между поглощением света и концентрацией. Это связано с тем, что процесс излучения является вторичным и зависит от предшествующего ему процесса поглощения света. Рассмотрим простейший случай, когда в растворе находится только одно флуоресцирующее вещество. Таким образом: Следовательно, зависимость между интенсивностью флуоресценции и концентрацией флуоресцирующего вещества не является линейной.
Функцию можно разложить в ряд Маклорена Если произведение (оптическая плотность раствора) невелико, то и тогда Таким образом, при малых значениях оптической плотности
(при l возб) зависимость интенсивности флуоресценции от концентрации можно считать линейной
, что и используется в количественном анализе. При более высоких значениях A зависимость интенсивности флуоресценции от концентрации становится более сложной и отклоняется от линейной. При A = 0,01 отклонение от линейности составляет 1%, 0,05 - 5%; 0,5 - около 35% (рис. 21.4). Рис. 21.4.
Зависимость между интенсивностью флуоресценции и оптической плотностью раствора
1) рассчитанная по упрощённой формуле I = KC; 2) реальная Влияние оптической плотности раствора на интенсивность флуоресценции называется «эффектом внутреннего фильтра
». Этот эффект обусловлен двумя причинами: · поглощением возбуждающего света
, вследствие чего частицы, находящиеся дальше от источника излучения, будут получать меньше возбуждающего излучения; · поглощением
одними частицами вещества излучения
, испускаемого другими частицами этого же вещества.![]() где - интегрируемая по Лебегу функция. Функция называется плотностью распределения случайной величины.
где - интегрируемая по Лебегу функция. Функция называется плотностью распределения случайной величины.![]()
![]()
пример: количество пассажиров в транспорте.
пример: время, масса, объем, температура тела.
1). Плотность вероятности является неотрицательной функцией: f(x)>0
2) вероятность того, что в результате испытания непрерыв. Случ. Величина примет какое-либо значение из интервала(а,b), равна определенному интегралу(в пределах от а до b) от плотности вероятности этой случайной величины. ![]()
![]()
![]() , когда выборка имеет распределение с плотностью
, когда выборка имеет распределение с плотностью ![]() . Предположим, что есть убывающая функция от параметра . Обозначим квантиль распределения , тогда есть возрастающая функция от . Зафиксируем близкое к нулю положительное число (например, 0,05 или 0,01). Пусть . При каждом неравенства
. Предположим, что есть убывающая функция от параметра . Обозначим квантиль распределения , тогда есть возрастающая функция от . Зафиксируем близкое к нулю положительное число (например, 0,05 или 0,01). Пусть . При каждом неравенства![]()
![]()

i
-тый отобранный объект (i
= 1,2,...n
)представлен парой чисел x i
, y i
: x
1
x
2
...
x n
y
1
y
2
...
y n

 ,
,  ,
, .
.
Dx i
= D
x i
s
n
параметра D
генеральной совокупности называетсясостоятельной
, если она сходится по вероятности к D.
Это означает, что для любых положительных чисел e
иg
найдется такое число n e g
, что для всех чисел n
, удовлетворяющих неравенству n > n e g
выполняется условие ![]() . и являются несмещёнными, состоятельными и эффективными оценками величин Mx
и Dx
.
. и являются несмещёнными, состоятельными и эффективными оценками величин Mx
и Dx
.

 Рис. 29.2.
Независимость спектра люминесценции от длины волны возбуждающего света
Рис. 29.2.
Независимость спектра люминесценции от длины волны возбуждающего света По методике исследования люминесцентный анализ можно представить следующей схемой.
По методике исследования люминесцентный анализ можно представить следующей схемой. Макроанализ -
наблюдение невооруженным глазом люминесценции объектов, облученных УФ-излучением:
Макроанализ -
наблюдение невооруженным глазом люминесценции объектов, облученных УФ-излучением:

 Люминесцения: основные понятия ■ Итак, что такое люминесценция? Определение этого понятия довольно сложно и исходит из сопоставления свойств люминесцентного излучения и законов теплового равновесного излучения. Под тепловым излучением понимают электромагнитное излучение, обусловленное возбуждением частиц вещества (атомов, молекул, ионов) вследствие их теплового движения. Чтобы вызвать люминесценцию вещества к нему необходимо подвести извне определенное количество энергии. ■ Люминесценция – это свечение атомов, молекул и других более сложных комплексов, возникающего в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в нормальное (В. Л. Левшин).
Люминесцения: основные понятия ■ Итак, что такое люминесценция? Определение этого понятия довольно сложно и исходит из сопоставления свойств люминесцентного излучения и законов теплового равновесного излучения. Под тепловым излучением понимают электромагнитное излучение, обусловленное возбуждением частиц вещества (атомов, молекул, ионов) вследствие их теплового движения. Чтобы вызвать люминесценцию вещества к нему необходимо подвести извне определенное количество энергии. ■ Люминесценция – это свечение атомов, молекул и других более сложных комплексов, возникающего в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в нормальное (В. Л. Левшин). Люминесцения: основные понятия ■ Люминесценция – это излучение (B`v, T), представляющее собой избыток над тепловым излучением (Bv, T) вещества при данной температуре и имеющее длительность (>10 -10 c), значительно превышающую период световых волн (Видеман - Вавилов).
Люминесцения: основные понятия ■ Люминесценция – это излучение (B`v, T), представляющее собой избыток над тепловым излучением (Bv, T) вещества при данной температуре и имеющее длительность (>10 -10 c), значительно превышающую период световых волн (Видеман - Вавилов).


 Основные характеристики люминесценции n Спектры поглощения: A = f(λ); A = f(v); T, % = f(λ); T, % = f(v). n Cпектры люминесценции: I = f(λ); I = f(v). n Спектры возбуждения: зависимости интенсивности люминесценции (I) от частоты (волнового числа) или длины волны возбуждающего света; у частиц, люминесцирующих по типу дискретных центров, спектры возбуждения идентичны спектрам поглощения. n Энергетический выход люминесценции. n Квантовый выход люминесценции. n Время жизни возбужденного люминесцентного центра.
Основные характеристики люминесценции n Спектры поглощения: A = f(λ); A = f(v); T, % = f(λ); T, % = f(v). n Cпектры люминесценции: I = f(λ); I = f(v). n Спектры возбуждения: зависимости интенсивности люминесценции (I) от частоты (волнового числа) или длины волны возбуждающего света; у частиц, люминесцирующих по типу дискретных центров, спектры возбуждения идентичны спектрам поглощения. n Энергетический выход люминесценции. n Квантовый выход люминесценции. n Время жизни возбужденного люминесцентного центра.






 Выход люминесценции n Способность вещества к люминесценции в данной среде характеризуется величиной выхода люминесценции. n Различают абсолютный квантовый и энергетический выходы люминесценции и относительный выход люминесценции. n Абсолютным квантовым выходом люминесценции (φкв) называют отношение числа квантов Nл, излученных веществом, к числу поглощенных квантов возбуждающего света Nп: φкв = Nл / Nп ■ φкв определяется соотношением между вероятностями излучательного (α) и безызлучательного (β): φкв = α / α + β
Выход люминесценции n Способность вещества к люминесценции в данной среде характеризуется величиной выхода люминесценции. n Различают абсолютный квантовый и энергетический выходы люминесценции и относительный выход люминесценции. n Абсолютным квантовым выходом люминесценции (φкв) называют отношение числа квантов Nл, излученных веществом, к числу поглощенных квантов возбуждающего света Nп: φкв = Nл / Nп ■ φкв определяется соотношением между вероятностями излучательного (α) и безызлучательного (β): φкв = α / α + β Выход люминесценции n Абсолютным энергетическим выходом люминесценции (φэн) называют отношение излучаемой веществом энергии Ел к поглощенной энергии возбуждения Еп: φэн = Ел / Еп ■ Абсолютный энергетический и квантовые выходы связаны простым соотношением: φэн = Ел / Еп = Nл hvл / Nп hvп = φкв (vл / vп) или φэн = φкв (λп / λл); φкв = φэн (λл / λп) ■ Измерение абсолютных выходов люминесценции представляет трудную задачу, поэтому на практике чаще измеряют относительный выход люминесценции.
Выход люминесценции n Абсолютным энергетическим выходом люминесценции (φэн) называют отношение излучаемой веществом энергии Ел к поглощенной энергии возбуждения Еп: φэн = Ел / Еп ■ Абсолютный энергетический и квантовые выходы связаны простым соотношением: φэн = Ел / Еп = Nл hvл / Nп hvп = φкв (vл / vп) или φэн = φкв (λп / λл); φкв = φэн (λл / λп) ■ Измерение абсолютных выходов люминесценции представляет трудную задачу, поэтому на практике чаще измеряют относительный выход люминесценции. Время жизни возбужденного люминесцентного центра n В случае люминесцентных дискретных центров число возбужденных центров n после прекращения возбуждения в отсутствии безызлучательных процессов дезактивации будет уменьшаться со временем: -dn/dt = k 1 n, где k 1 – константа скорости мономолекулярного излучательного процесса. ■ Среднее излучательное время жизни (τ0) люминесцентного центра определяется выражением: τ0 = 1/ k 1
Время жизни возбужденного люминесцентного центра n В случае люминесцентных дискретных центров число возбужденных центров n после прекращения возбуждения в отсутствии безызлучательных процессов дезактивации будет уменьшаться со временем: -dn/dt = k 1 n, где k 1 – константа скорости мономолекулярного излучательного процесса. ■ Среднее излучательное время жизни (τ0) люминесцентного центра определяется выражением: τ0 = 1/ k 1 Время жизни возбужденного люминесцентного центра n Для грубых оценок применимо соотношение: 10 -4 τ0 ≈ ---- ε(λmax) n Таким образом, среднее излучательное время жизни возбужденного состояния тем меньше, чем интенсивнее поглощение, приводящее к его возникновению. n Поскольку имеют место безызлучательные процессы, измеряемые времена жизни τ всегда меньше τ0: 1 τ = ------ k 1 + k 2 + k 3
Время жизни возбужденного люминесцентного центра n Для грубых оценок применимо соотношение: 10 -4 τ0 ≈ ---- ε(λmax) n Таким образом, среднее излучательное время жизни возбужденного состояния тем меньше, чем интенсивнее поглощение, приводящее к его возникновению. n Поскольку имеют место безызлучательные процессы, измеряемые времена жизни τ всегда меньше τ0: 1 τ = ------ k 1 + k 2 + k 3 Энергетические переходы в молекуле n При комнатной температуре молекула обычно находится в n n основном S 0 синглетном состоянии. При поглощении энергии молекула оказывается в возбужденном электронном состоянии S 2. Далее практически мгновенно (~10 -12 с) в результате колебательной релаксации (КР) достигается невозбужденный колебательный уровень S 2. Далее также практически мгновенно (~10 -11 с) вследствие внутренней конверсии молекула перейдет в более низкое электронно-возбужденное состояние S 1. Переход S 1 → S 0 с испусканием фотона (10 -6 - 10 -9 с) – флуоресценция.
Энергетические переходы в молекуле n При комнатной температуре молекула обычно находится в n n основном S 0 синглетном состоянии. При поглощении энергии молекула оказывается в возбужденном электронном состоянии S 2. Далее практически мгновенно (~10 -12 с) в результате колебательной релаксации (КР) достигается невозбужденный колебательный уровень S 2. Далее также практически мгновенно (~10 -11 с) вследствие внутренней конверсии молекула перейдет в более низкое электронно-возбужденное состояние S 1. Переход S 1 → S 0 с испусканием фотона (10 -6 - 10 -9 с) – флуоресценция.



 Энергетические переходы в молекуле ■ Безызлучательный переход S 1 → T 1 с изменением спина электрона – интеркомбинационная конверсия. n Переход T 1 → S 0 с испусканием фотона (>10 -4 c) – фосфоресценция.
Энергетические переходы в молекуле ■ Безызлучательный переход S 1 → T 1 с изменением спина электрона – интеркомбинационная конверсия. n Переход T 1 → S 0 с испусканием фотона (>10 -4 c) – фосфоресценция. Замедленная флуоресценция n Помимо флуоресценции и фосфоресценции существует еще один вид люминесценции – замедленная флуоресценция. n Этот вид молекулярной люминесценции наблюдается в весьма ограниченных диапазонах температур, вязкостей и концентраций растворов. n По сравнению с флуоресценцией и фосфоресценцией ее интенсивность невелика и достигает максимальных значений при комнатной и более высоких температурах, заметно ослабевая с понижением температуры. n Различают замедленную флуоресценцию Е – типа.
Замедленная флуоресценция n Помимо флуоресценции и фосфоресценции существует еще один вид люминесценции – замедленная флуоресценция. n Этот вид молекулярной люминесценции наблюдается в весьма ограниченных диапазонах температур, вязкостей и концентраций растворов. n По сравнению с флуоресценцией и фосфоресценцией ее интенсивность невелика и достигает максимальных значений при комнатной и более высоких температурах, заметно ослабевая с понижением температуры. n Различают замедленную флуоресценцию Е – типа. Замедленная флуоресценция Е - типа n Замедленная флуоресценция Е – типа: за счет термической активации молекул в состоянии Т 1 происходит их переход на более высокие колебательные уровни, которые могут перекрываться с колебательными уровнями S 1 и и становится возможным переход Т 1 → S 1.
Замедленная флуоресценция Е - типа n Замедленная флуоресценция Е – типа: за счет термической активации молекул в состоянии Т 1 происходит их переход на более высокие колебательные уровни, которые могут перекрываться с колебательными уровнями S 1 и и становится возможным переход Т 1 → S 1. Замедленная флуоресценция n Замедленная флуоресценция Р - типа (наблюдаемая у молекул пирена и других ароматических соединений): возникает при переносе энергии в результате столкновений
Замедленная флуоресценция n Замедленная флуоресценция Р - типа (наблюдаемая у молекул пирена и других ароматических соединений): возникает при переносе энергии в результате столкновений Диаграмма потенциальной энергии n При рассмотрении люминесценции полезно рассмотрение диаграммы потенциальной энергии. n Ограничимся двумерными диаграммами, относящимися, строго говоря, к случаю двухатомной молекулы.
Диаграмма потенциальной энергии n При рассмотрении люминесценции полезно рассмотрение диаграммы потенциальной энергии. n Ограничимся двумерными диаграммами, относящимися, строго говоря, к случаю двухатомной молекулы. Диаграмма потенциальной энергии n Кривые потенциальной энергии состояний S 1 и T 1 пересекаются в некоторой точке. n В этой точке положение и импульсы атомных ядер одни и те же, т. е. возможен S 1 → T 1 переход. n В сложных многоатомных молекулах многомерные потенциальные поверхности могут пересекаться во многих точках, что увеличивает вероятность ИК. n Принцип Франка – Кондона. Согласно этому принципу электронные переходы являются настолько быстрыми процессами (10 -13 с) по сравнению с движением ядер (10 -12 с), что за время электронного перехода ядра не успевают изменить ни своей скорости ни своего взаимного расположения.
Диаграмма потенциальной энергии n Кривые потенциальной энергии состояний S 1 и T 1 пересекаются в некоторой точке. n В этой точке положение и импульсы атомных ядер одни и те же, т. е. возможен S 1 → T 1 переход. n В сложных многоатомных молекулах многомерные потенциальные поверхности могут пересекаться во многих точках, что увеличивает вероятность ИК. n Принцип Франка – Кондона. Согласно этому принципу электронные переходы являются настолько быстрыми процессами (10 -13 с) по сравнению с движением ядер (10 -12 с), что за время электронного перехода ядра не успевают изменить ни своей скорости ни своего взаимного расположения. Принцип Франка - Кондона n Поэтому прежнее положение ядер будет соответствовать изменившимся в результате электронного перехода силам только в том случае, если молекула будет совершать достаточные колебания. n Так, при электронном возбуждении молекулы прочность связи мгновенно ослабевает, а ядра в первый момент продолжают занимать прежнее близкое друг к другу положение (сжатая молекула). n Такое несоответствие приводит к тому, что молекула начинает совершать колебания. n За короткое время жизни возбужденного состояния (10 -9 с) избыточная колебательная энергия успевает распределиться между многочисленными колебаниями молекулы или передаться окружающей среде.
Принцип Франка - Кондона n Поэтому прежнее положение ядер будет соответствовать изменившимся в результате электронного перехода силам только в том случае, если молекула будет совершать достаточные колебания. n Так, при электронном возбуждении молекулы прочность связи мгновенно ослабевает, а ядра в первый момент продолжают занимать прежнее близкое друг к другу положение (сжатая молекула). n Такое несоответствие приводит к тому, что молекула начинает совершать колебания. n За короткое время жизни возбужденного состояния (10 -9 с) избыточная колебательная энергия успевает распределиться между многочисленными колебаниями молекулы или передаться окружающей среде. Принцип Франка - Кондона n В результате молекула из неравновесного Франк – Кондоновского состояния переходит в равновесное, в котором ядра в соответствии с ослабленной связью разнесены друг от друга и совершают относительно этого положения колебания. n Далее – при испускании кванта люминесценции прочность связи в молекуле мгновенно усиливается, ядра же в первый момент продолжают занимать прежнее, далекое друг от друга положение (растянутая молекула). n И снова – переход из неравновесного Франк - Кондоновского состояния в равновесное осуществляется в результате колебаний.
Принцип Франка - Кондона n В результате молекула из неравновесного Франк – Кондоновского состояния переходит в равновесное, в котором ядра в соответствии с ослабленной связью разнесены друг от друга и совершают относительно этого положения колебания. n Далее – при испускании кванта люминесценции прочность связи в молекуле мгновенно усиливается, ядра же в первый момент продолжают занимать прежнее, далекое друг от друга положение (растянутая молекула). n И снова – переход из неравновесного Франк - Кондоновского состояния в равновесное осуществляется в результате колебаний. Принцип Франка - Кондона n Итак, согласно принципу Франка - Кондона, при электронном возбуждении внутримолекулярные связи, как правило, ослабляются. n Это приводит к тому, что минимум потенциальной кривой возбужденного состояния расположен при несколько большем межъядерном расстоянии, чем у основного состояния. n Как следует из квантовой механики, наиболее вероятное межъядерное расстояние для молекулы с нулевой колебательной энергией соответствует средней точке АВ или CD.
Принцип Франка - Кондона n Итак, согласно принципу Франка - Кондона, при электронном возбуждении внутримолекулярные связи, как правило, ослабляются. n Это приводит к тому, что минимум потенциальной кривой возбужденного состояния расположен при несколько большем межъядерном расстоянии, чем у основного состояния. n Как следует из квантовой механики, наиболее вероятное межъядерное расстояние для молекулы с нулевой колебательной энергией соответствует средней точке АВ или CD. Принцип Франка - Кондона n Наиболее вероятными будут переходы, отвечающие вертикальным линиям, проведенным из середины отрезков АВ (поглощение)или CD (испускание) до пересечения с соответствующими потенциальными кривыми:
Принцип Франка - Кондона n Наиболее вероятными будут переходы, отвечающие вертикальным линиям, проведенным из середины отрезков АВ (поглощение)или CD (испускание) до пересечения с соответствующими потенциальными кривыми:
 Фотолюминесценция n Способность веществ к люминесценции, как и к поглощению излучения, связана с их электронным строением. n Например, если низшее возбужденное синглетное состояние органической молекулы обусловлено π → π* переходом, то она часто имеет высокие выходы и флуоресценции и фосфоресценции. n В тех же случаях, когда низшее возбужденное синглетное состояние возникает в результате n → π* перехода, то молекула обычно обладает малым выходом флуоресценции, но может обладать высоким выходом фосфоресценции при низкой температуре. n Обычно переход n → π* является наиболее длинноволновым переходом.
Фотолюминесценция n Способность веществ к люминесценции, как и к поглощению излучения, связана с их электронным строением. n Например, если низшее возбужденное синглетное состояние органической молекулы обусловлено π → π* переходом, то она часто имеет высокие выходы и флуоресценции и фосфоресценции. n В тех же случаях, когда низшее возбужденное синглетное состояние возникает в результате n → π* перехода, то молекула обычно обладает малым выходом флуоресценции, но может обладать высоким выходом фосфоресценции при низкой температуре. n Обычно переход n → π* является наиболее длинноволновым переходом.

 Фотолюминесценция n Вероятность такого перехода мала (ε λmax ~ (1 - 2) 103 M -1 см-1), а время жизни возбужденного синглетного состояния n , π*, а значит и вероятность безызлучательной дезактивации велики. n Экспериментально установлено, что разница в энергиях S 1 ↔ T 1 для состояния n , π* в 2 - 4 раза меньше, чем для состояния π, π*. n Все это приводит к тому, что часто соединения, содержащие n - электроны, слабо или вовсе не флуоресцируют, но сильно фосфоресцируют.
Фотолюминесценция n Вероятность такого перехода мала (ε λmax ~ (1 - 2) 103 M -1 см-1), а время жизни возбужденного синглетного состояния n , π*, а значит и вероятность безызлучательной дезактивации велики. n Экспериментально установлено, что разница в энергиях S 1 ↔ T 1 для состояния n , π* в 2 - 4 раза меньше, чем для состояния π, π*. n Все это приводит к тому, что часто соединения, содержащие n - электроны, слабо или вовсе не флуоресцируют, но сильно фосфоресцируют.
 Структура и оптические свойства молекул n Замечено, что наибольшей способностью к люминесценции обладают симметричные молекулы с протяженной системой сопряженных связей, склонные к образованию орто - и пара - хиноидных колец. n Одним из наиболее важных факторов, обуславливающих люминесценцию, является требование о наличии жесткой и плоской структуры. n По - видимому, относительное вращение частей «гибкой» молекулы возмущает электронные оболочки и облегчает безызлучательные переходы. n Например, известный гормон адреналин не люминесцирует, но при окислении превращается в ярко люминесцирующий триоксидон.
Структура и оптические свойства молекул n Замечено, что наибольшей способностью к люминесценции обладают симметричные молекулы с протяженной системой сопряженных связей, склонные к образованию орто - и пара - хиноидных колец. n Одним из наиболее важных факторов, обуславливающих люминесценцию, является требование о наличии жесткой и плоской структуры. n По - видимому, относительное вращение частей «гибкой» молекулы возмущает электронные оболочки и облегчает безызлучательные переходы. n Например, известный гормон адреналин не люминесцирует, но при окислении превращается в ярко люминесцирующий триоксидон.
 Структура и оптические свойства молекул n Люминесцирующий флуоресцеин отличается от нелюминесцирующего фенолфталеина только тем, что в молекуле флуоресцеина кислородный мостик жестко удерживает два кольца в одной плоскости: флуоресцеин фенолфталеин
Структура и оптические свойства молекул n Люминесцирующий флуоресцеин отличается от нелюминесцирующего фенолфталеина только тем, что в молекуле флуоресцеина кислородный мостик жестко удерживает два кольца в одной плоскости: флуоресцеин фенолфталеин Основные закономерности молекулярной люминесценции n Правило Каши: форма спектра люминесценции не зависит от длины волны возбуждающего света. n Закон Стокса - Ломмеля: спектр люминесценции в целом и его максимум сдвинут со спектром поглощения и его максимумом в длинноволновую область. n Правило Левшина (правило зеркальной симметрии): нормированные спектры поглощения и флуоресценции, представленные в виде графиков ε = f(v) и I/v = f(v), зеркально симметричны относительно прямой, перпендикулярной к оси частот и проходящей через точку пересечения спектров v 0.
Основные закономерности молекулярной люминесценции n Правило Каши: форма спектра люминесценции не зависит от длины волны возбуждающего света. n Закон Стокса - Ломмеля: спектр люминесценции в целом и его максимум сдвинут со спектром поглощения и его максимумом в длинноволновую область. n Правило Левшина (правило зеркальной симметрии): нормированные спектры поглощения и флуоресценции, представленные в виде графиков ε = f(v) и I/v = f(v), зеркально симметричны относительно прямой, перпендикулярной к оси частот и проходящей через точку пересечения спектров v 0. Основные закономерности молекулярной люминесценции n Правило Левшина: va + vf = 2 v 0, где va, vf – симметричные частоты поглощения и флуоресценции; v 0 – частота чисто электронного перехода, т. е. перехода между нулевыми колебательными уровнями S 0 ↔ S 1; ∆v = va - vf = 2(va - v 0)
Основные закономерности молекулярной люминесценции n Правило Левшина: va + vf = 2 v 0, где va, vf – симметричные частоты поглощения и флуоресценции; v 0 – частота чисто электронного перехода, т. е. перехода между нулевыми колебательными уровнями S 0 ↔ S 1; ∆v = va - vf = 2(va - v 0) Основные закономерности молекулярной люминесценции n Закон Вавилова: по мере увеличения λв энергетический выход флуоресценции возрастает, сохраняет постоянную величину и затем уменьшается.
Основные закономерности молекулярной люминесценции n Закон Вавилова: по мере увеличения λв энергетический выход флуоресценции возрастает, сохраняет постоянную величину и затем уменьшается.
 Закон затухания люминесценции n Для интенсивности люминесценции Iл, определяемой скоростью испускания квантов люминесценции, имеем: dn Iл = - --- = k 1 n 0 e-k 1 t = Iл 0 e-k 1 t, dt где Iл 0 – интенсивность люминесценции в первый момент после прекращения возбуждения. n Таким образом, интенсивность люминесценции дискретного центра уменьшается со временем по экспоненциальному закону. n Затухание рекомбинационного свечения происходит по более сложному гиперболическому закону.
Закон затухания люминесценции n Для интенсивности люминесценции Iл, определяемой скоростью испускания квантов люминесценции, имеем: dn Iл = - --- = k 1 n 0 e-k 1 t = Iл 0 e-k 1 t, dt где Iл 0 – интенсивность люминесценции в первый момент после прекращения возбуждения. n Таким образом, интенсивность люминесценции дискретного центра уменьшается со временем по экспоненциальному закону. n Затухание рекомбинационного свечения происходит по более сложному гиперболическому закону. Зависимость интенсивности люминесценции от концентрации n При стационарном (непрерывном) возбуждении образца и отсутствии тушения: Iл = k 1 φкв Nп (Nп – число поглощенных квантов); Nп = k 2 (I 0 – I); I = I 0 10 -εℓC; Iл = k φкв I 0 (1 - 10 -εℓC), где k – коэффициент пропорциональности; Разложение 10 -εℓC в ряд дает: (2, 3εℓC) 2 (2, 3εℓC)3 1 - 2, 3εℓC + ---- - ---- + ……. ; 2! 3!
Зависимость интенсивности люминесценции от концентрации n При стационарном (непрерывном) возбуждении образца и отсутствии тушения: Iл = k 1 φкв Nп (Nп – число поглощенных квантов); Nп = k 2 (I 0 – I); I = I 0 10 -εℓC; Iл = k φкв I 0 (1 - 10 -εℓC), где k – коэффициент пропорциональности; Разложение 10 -εℓC в ряд дает: (2, 3εℓC) 2 (2, 3εℓC)3 1 - 2, 3εℓC + ---- - ---- + ……. ; 2! 3! Зависимость интенсивности люминесценции от концентрации ■ При εℓC ≤ 10 -2 вклад третьего и последующих членов разложения незначительны: Iл = 2, 3 k φкв I 0 ε ℓ C; Iл = k C; обычно ε ~ 103 – 104, тогда при ℓ = 1 см Сi = 10 -5 – 10 -6 M
Зависимость интенсивности люминесценции от концентрации ■ При εℓC ≤ 10 -2 вклад третьего и последующих членов разложения незначительны: Iл = 2, 3 k φкв I 0 ε ℓ C; Iл = k C; обычно ε ~ 103 – 104, тогда при ℓ = 1 см Сi = 10 -5 – 10 -6 M Причины отклонения зависимости Iл = k. C от линейности ■ Эффект внутреннего фильтра связан с поглощением части возбуждающего излучения при прохождении через слой люминофора; ■ Самопоглощение – поглощение люминофором части люминесцентного излучения; ■ Тушение люминесценции: концентрационное тушение (образование нелюминесцирующих агрегатов, миграция энергии от возбужденных молекул к невозбужденным); температурное тушение (внутримолекулярный процесс, обусловленный значительным увеличением колебательной энергии при повышении Т);
Причины отклонения зависимости Iл = k. C от линейности ■ Эффект внутреннего фильтра связан с поглощением части возбуждающего излучения при прохождении через слой люминофора; ■ Самопоглощение – поглощение люминофором части люминесцентного излучения; ■ Тушение люминесценции: концентрационное тушение (образование нелюминесцирующих агрегатов, миграция энергии от возбужденных молекул к невозбужденным); температурное тушение (внутримолекулярный процесс, обусловленный значительным увеличением колебательной энергии при повышении Т); Тушение люминесценции ■ Тушение люминесценции: тушение посторонними веществами (тяжелые ионы: I-, Br-, Cs+, Cu+; парамагнитные Mn 2+, O 2; молекулы растворителя); статическое тушение (примесное вещество образует с невозбужденным люминофором нелюминесцирующие продукты); динамическое тушение (примесное вещество образует с возбужденным люминофором нелюминесцирующие продукты).
Тушение люминесценции ■ Тушение люминесценции: тушение посторонними веществами (тяжелые ионы: I-, Br-, Cs+, Cu+; парамагнитные Mn 2+, O 2; молекулы растворителя); статическое тушение (примесное вещество образует с невозбужденным люминофором нелюминесцирующие продукты); динамическое тушение (примесное вещество образует с возбужденным люминофором нелюминесцирующие продукты). Тушение люминесценции ■ Уравнение Штерна - Фольмера: φкв(Q) = k 1 / (k 1 + k 2 + k 3 [Q];
Тушение люминесценции ■ Уравнение Штерна - Фольмера: φкв(Q) = k 1 / (k 1 + k 2 + k 3 [Q];



 Практическое применение люминесценции Флуориметрические определения: cобственная люминесценция (UO 22+, комплексные галогениды тяжелых металлов Tl+, Sn 2+, Sb 3+, Te(IV), Pb 2+, Bi 3+, In 3+ и др. , кристаллофосфоры, органические соединения); флуоресценция комплексных соединений ионов металлов с органическими реагентами. ■ Фосфориметрические определения. ■ Временная селекция. ■ Синхронное сканирование спектров (производные спектры). ■ Хемилюминесцентный анализ. ■
Практическое применение люминесценции Флуориметрические определения: cобственная люминесценция (UO 22+, комплексные галогениды тяжелых металлов Tl+, Sn 2+, Sb 3+, Te(IV), Pb 2+, Bi 3+, In 3+ и др. , кристаллофосфоры, органические соединения); флуоресценция комплексных соединений ионов металлов с органическими реагентами. ■ Фосфориметрические определения. ■ Временная селекция. ■ Синхронное сканирование спектров (производные спектры). ■ Хемилюминесцентный анализ. ■
 Синхронные спектры ■ Синхронные спектры получают при одновременном (синхронном) сканировании (изменении) длин волн возбуждения и испускания с постоянным сдвигом Δλ между ними. ■ При этом наблюдается значительное упрощение спектров люминесценции сложных молекул, сужение их полос и, как следствие, повышение селективности определений, а также уменьшение фонового свечения за счет подавления релеевского и комбинационного рассеяния растворителя. ■ Оптимальным условием для достижения наиболее интенсивного сигнала и наименьшей полуширины линии является синхронное сканирование с условием: Δλ = λисп (макс.) - λвозб (макс.)
Синхронные спектры ■ Синхронные спектры получают при одновременном (синхронном) сканировании (изменении) длин волн возбуждения и испускания с постоянным сдвигом Δλ между ними. ■ При этом наблюдается значительное упрощение спектров люминесценции сложных молекул, сужение их полос и, как следствие, повышение селективности определений, а также уменьшение фонового свечения за счет подавления релеевского и комбинационного рассеяния растворителя. ■ Оптимальным условием для достижения наиболее интенсивного сигнала и наименьшей полуширины линии является синхронное сканирование с условием: Δλ = λисп (макс.) - λвозб (макс.)
 Трехмерные спектры ■ Трехмерные спектры представляют собой зависимость интенсивности люминесценции как от длины волны возбуждения, так и от длины волны испускания. ■ Трехмерные спектры имеют вид «горной гряды» . Каждая строка такой гряды представляет собой спектр излучения, а каждый столбец – спектр возбуждения. ■ Такие спектры получают из большого числа (обычно не менее 50) индивидуальных спектров люминесценции, записанных через определенные промежутки длин волн возбуждения. ■ Трехмерные спектры дают полную картину спектральных свойств исследуемого образца.
Трехмерные спектры ■ Трехмерные спектры представляют собой зависимость интенсивности люминесценции как от длины волны возбуждения, так и от длины волны испускания. ■ Трехмерные спектры имеют вид «горной гряды» . Каждая строка такой гряды представляет собой спектр излучения, а каждый столбец – спектр возбуждения. ■ Такие спектры получают из большого числа (обычно не менее 50) индивидуальных спектров люминесценции, записанных через определенные промежутки длин волн возбуждения. ■ Трехмерные спектры дают полную картину спектральных свойств исследуемого образца.
 Контурные (двумерные) спектры ■ Использование трехмерных спектров для анализа смесей, содержащих более трех компонентов, и имеющих широкие размытые полосы в одной и той же спектральной области, представляет неразрешимую задачу. ■ В данном случае более перспективным является использование контурных спектров – результат сечения трехмерного спектра плоскостями, параллельными плоскости ХОУ, с последующим объединением полученных сечений в одной плоскости ХОУ. ■ Получающиеся изображения напоминают контурные карты (контурные спектры), которые являются «отпечатками пальцев» индивидуального соединения.
Контурные (двумерные) спектры ■ Использование трехмерных спектров для анализа смесей, содержащих более трех компонентов, и имеющих широкие размытые полосы в одной и той же спектральной области, представляет неразрешимую задачу. ■ В данном случае более перспективным является использование контурных спектров – результат сечения трехмерного спектра плоскостями, параллельными плоскости ХОУ, с последующим объединением полученных сечений в одной плоскости ХОУ. ■ Получающиеся изображения напоминают контурные карты (контурные спектры), которые являются «отпечатками пальцев» индивидуального соединения.

 Хемилюминесцентный анализ ■ Хемилюминесцентный анализ основан на явлении хемилюминесценции (ХЛ). Этот вид свечения не требует внешнего источника возбуждения, а возникает за счет энергии экзотермических химических процессов: A + B → P* + C P* → P + hvcl n В растворах ХЛ наблюдается главным образом в реакциях окисления органических веществ кислородом или пероксидом водорода. n Образование продуктов реакции происходит чаще всего по сложному радикально-цепному механизму. n Так, многие полагают, что окисление люминола (I) протекает с участием радикалов HO 2*, HO*, O 2*.
Хемилюминесцентный анализ ■ Хемилюминесцентный анализ основан на явлении хемилюминесценции (ХЛ). Этот вид свечения не требует внешнего источника возбуждения, а возникает за счет энергии экзотермических химических процессов: A + B → P* + C P* → P + hvcl n В растворах ХЛ наблюдается главным образом в реакциях окисления органических веществ кислородом или пероксидом водорода. n Образование продуктов реакции происходит чаще всего по сложному радикально-цепному механизму. n Так, многие полагают, что окисление люминола (I) протекает с участием радикалов HO 2*, HO*, O 2*. Хемилюминесцентный анализ ■ Основные группы определяемых соединений: хемилюминесцентные соединения, которые при окислении излучают свет (люминол, люцигенин, лофин и др.); окислители (пероксид водорода, гипохлориты, гипобромиты, персулфаты, перманганат калия, молекулярный кислород и др.); катализаторы индикаторных реакций (ионы меди, кобальта, марганца, никеля, железа и др.); ингибиторы индикаторных реакций (ароматические соединения, содержащие фенольные и аминогруппы); соединения, изменяющие р. Н среды (щелочи, карбонаты, органические основания и др.). ■ Сортовой ХЛ анализ и индикаторные методы.
Хемилюминесцентный анализ ■ Основные группы определяемых соединений: хемилюминесцентные соединения, которые при окислении излучают свет (люминол, люцигенин, лофин и др.); окислители (пероксид водорода, гипохлориты, гипобромиты, персулфаты, перманганат калия, молекулярный кислород и др.); катализаторы индикаторных реакций (ионы меди, кобальта, марганца, никеля, железа и др.); ингибиторы индикаторных реакций (ароматические соединения, содержащие фенольные и аминогруппы); соединения, изменяющие р. Н среды (щелочи, карбонаты, органические основания и др.). ■ Сортовой ХЛ анализ и индикаторные методы.
 Хемилюминесцентный анализ ■ Сортовой ХЛ анализ применяется при испытаниях вин, соков плодов и овощей, мясных экстрактов и т. д. Так, по реакции окисления люминола в присутствии катализатора - комплекса ионов меди с α-аминокислотами, содержащимися в соке картофеля, можно улавливать сортовые различия картофеля: сорта различаются по содержанию аминокислот. ■ К индикаторным методам ХЛ анализа относятся различные виды титрования с использованием хемилюминесцентных индикаторов (ХЛИ). В отличии от флуоресцентных индикаторов для работы с ХЛИ не требуется источника возбуждения.
Хемилюминесцентный анализ ■ Сортовой ХЛ анализ применяется при испытаниях вин, соков плодов и овощей, мясных экстрактов и т. д. Так, по реакции окисления люминола в присутствии катализатора - комплекса ионов меди с α-аминокислотами, содержащимися в соке картофеля, можно улавливать сортовые различия картофеля: сорта различаются по содержанию аминокислот. ■ К индикаторным методам ХЛ анализа относятся различные виды титрования с использованием хемилюминесцентных индикаторов (ХЛИ). В отличии от флуоресцентных индикаторов для работы с ХЛИ не требуется источника возбуждения. Хемилюминесцентный анализ (аналитические характеристики) ■ Большей частью ХЛ – определения отличаются высокой чувствительностью: пределы обнаружения 10 -10 – 10 -4 г/мл при конечном объеме 2 – 5 мл. ■ Селективность ХЛ – определений, как правило, невысока, так как многие вещества влияют на скорость индикаторной реакции. Однако варьирование условий определения или применение маскирующих агентов позволяет «смягчить» этот недостаток. ■ Простота, доступность и дешевизна аппаратуры, используемой в ХЛ, в сочетании с возможностью экспрессного, высокочувствительного, а при определенных условиях, и селективного определения большого круга соединений обуславливает распространенность ХЛ.
Хемилюминесцентный анализ (аналитические характеристики) ■ Большей частью ХЛ – определения отличаются высокой чувствительностью: пределы обнаружения 10 -10 – 10 -4 г/мл при конечном объеме 2 – 5 мл. ■ Селективность ХЛ – определений, как правило, невысока, так как многие вещества влияют на скорость индикаторной реакции. Однако варьирование условий определения или применение маскирующих агентов позволяет «смягчить» этот недостаток. ■ Простота, доступность и дешевизна аппаратуры, используемой в ХЛ, в сочетании с возможностью экспрессного, высокочувствительного, а при определенных условиях, и селективного определения большого круга соединений обуславливает распространенность ХЛ.
Свойство
Объяснение
Спектр люминесценции не зависит от длины волны возбуждающего света (правило М.Каши)
Независимо от того, в какое возбуждённое состояние перешла молекула при поглощении фотона, испускание всегда происходит при переходе между первым возбуждённым и основным энергетическими уровнями
Как правило, спектр люминесценции в целом и его максимум всегда сдвинуты по сравнению со спектром поглощения и его максимумом в сторону больших длин волн (меньших энергий) - правило Стокса-Ломмеля
Часть поглощённой энергии теряется за счёт колебательной релаксации при столкновении с другими молекулами, кроме того, растворитель стабилизирует возбуждённое состояние и уменьшает его энергию
Для многих веществ нормированные спектры поглощения (только самая длинноволновая полоса) и флуоресценции, изображённые в функции частот или волновых чисел, симметричны относительно прямой, проходящей перпендикулярной оси абсцисс через точку пересечения этих спектров (правило В.Л. Лёвшина)
Поглощение (самая длинноволновая полоса) и испускание вызваны одними и теми же переходами (S 0 S 1 для флуоресценции)