Чтобы пользоваться предварительным просмотром презентаций создайте себе аккаунт (учетную запись) Google и войдите в него: https://accounts.google.com
Подписи к слайдам:
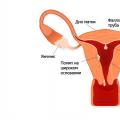
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.
Цель урока: 1. на основе положения металлов в ПСХЭ прийти к пониманию особенностей строения их атомов и кристаллов (металлической химической связи и кристаллической металлической решетки). 2.Обобщить и расширить знания о физических свойствах металлов и их классификаций. 3. Развивать умение анализировать, делать выводы исходя из положения металлов в периодической системе химических элементов.
МЕДЬ Иду на мелкую монету, В колоколах люблю звенеть, Мне ставят памятник за это И знают: имя мое-….
ЖЕЛЕЗО Пахать и строить - все он может, если ему уголек в том поможет…
Металлы – это группа веществ с общими свойствами.
Металлами являются элементы I – III групп главных подгрупп, и IV-VIII групп побочных подгрупп I группа II группа III группа IV группа V группа VI группа VII группа VIII группа Na Mg Al Ti V Cr Mn Fe
Из 109 элементов ПСХЭ 85 являются металлами: выделены голубым, зелёным и розовым цветом (кроме H и He)
Положение элемента в ПС отражает строение его атомов ПОЛОЖЕНИЕ ЭЛЕМЕНТА В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ СТРОЕНИЕ ЕГО АТОМОВ Порядковый номер элемента в периодической системе Заряд ядра атома Общее число электронов Номер группы Число электронов на внешнем энергетическом уровне. Высшая валентность элемента, степень окисления Номер периода Число энергетических уровней. Число подуровней на внешнем энергетическом уровне
Модель атома натрия
Электронное строение атома натрия
Задание 2. Составьте схему электронного строения атома алюминия и кальция в тетради самостоятельно по примеру с атомом натрия.
Вывод: 1. Металлы – элементы, имеющие на внешнем энергетическом уровне 1-3 электрона, реже 4-6. 2. Металлы – это химические элементы атомы которых отдают электроны внешнего (а иногда предвнешнего) электронного слоя превращаясь в положительные ионы. Металлы – восстановители. Это обусловлено небольшим числом электронов внешнего слоя, большим радиусом атомов, вследствие чего эти электроны слабо удерживаются с ядром.
Металлическая химическая связь характеризуется: - делокализацией связи, т.к. сравнительно небольшое количество электронов одновременно связывают множество ядер; - валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален; - металлическая связь не обладает направленностью и насыщенностью.
Кристаллические решетки металлов
Видеоинформация о кристаллах металлов
Свойства металлов определяются строением их атомов. Свойство металла Характеристика свойства твердость Все металлы кроме ртути, при обычных условиях твердые вещества. Самые мягкие – натрий, калий. Их можно резать ножом; самый твердый хром – царапает стекло. плотность Металлы делятся на лёгкие (плотность 5г/см) и тяжелые (плотность больше 5г/см). плавкость Металлы делятся на легкоплавкие и тугоплавкие электропроводность, теплопроводность Хаотически движущиеся электроны под действием электрического напряжения приобретают направленное движение, в результате чего возникает электрический ток. металлический блеск Электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают как стекло пластичность. Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и не сопровождается разрывом связи, и поэтому металл характеризуется высокой пластичностью.
Проверьте усвоение знаний на уроке тестированием 1) Электронная формула кальция. А) 1S 2 2S 2 2Р 6 3S 1 Б) 1S 2 2S 2 2 Р 6 3 S 2 В) 1S 2 2S 2 2 Р 6 3 S 2 3S 6 4S 1 Г) 1S 2 2S 2 2 Р 6 3 S 2 3 Р 6 4 S 2
Задания теста 2 и 3 2) Электронную формулу 1S 2 2S 2 2Р 6 3S 2 3Р 6 4S 2 имеет атом: а) Nа б) Са в) Сu г) Zn 3) Электропроводность, металлический блеск, пластичность, плотность металлов определяются: а) массой атомов б) температурой плавления металлов в) строением атомов металлов г) наличием неспаренных электронов
Задания теста 4 и 5 4) Металлы при взаимодействии с неметаллами проявляют свойства а) окислительные; б) восстановительные; в) и окислительные, и восстановительные; г) не участвуют в окислительно-восстановительных реакциях; 5) В периодической системе типичные металлы расположены в: а) верхней части; б) нижней части; в) правом верхнем углу; г) левом нижнем углу;
Правильные ответы Номер задания Вариант правильного ответа 1 Г 2 Б 3 В 4 Б 5 Г
Предварительный просмотр:
Цель и задачи урока:
- На основе положения металлов в ПСХЭ подвести учащихся к пониманию особенностей строения их атомов и кристаллов (металлической химической связи и кристаллической металлической решетки), изучить общие физические свойства металлов. Повторить и обобщить знания о химической связи и металлической кристаллической решетке.
- Развивать умение анализировать, делать выводы о строении атомов исходя из положения металлов в ПСХЭ.
- Развивать умение владеть химической терминологией, чётко формулировать и высказывать свои мысли.
- Воспитывать самостоятельность мышления в ходе учебной деятельности.
- Формировать интерес к будущей профессии.
Форма урока:
комбинированный урок с применением презентации
Методы и приёмы:
Рассказ, беседа, демонстрация видео типов кристаллических решеток металлов, тест, составление схем электронного строения атомов, демонстрация коллекции образцов металлов и сплавов.
Оборудование:
- Таблица «Периодическая система химических элементов Д.И. Менделеева»;
- Презентация урока на электронном носителе.
- Коллекция образцов металлов и сплавов.
- Проектор.
- Карточки с таблицей «Характеристика строения атома по положению в ПСХЭ»
ХОД УРОКА
I. Организационный момент урока .
II. Постановка и оглашение темы урока, его целей и задач.
Слайд 1-2
III. Изучение нового материала.
Учитель: Человек использовал металлы с древних времён. Кратко об истории использования металлов.
Сообщение 1 учащегося. Слайд 3
В начале был век медный .
К концу каменного века человек открыл возможность использования металлов для изготовления орудий труда. Первым таким металлом была медь.
Период распространения медных орудий называют энеолитом или халколитом , что в переводе с греческого означает «медь». Медь обрабатывалась с помощью каменных орудий методом холодной ковки. Самородки меди превращались в изделия под тяжелыми ударами молота. В начале медного века из меди делали лишь мягкие орудия, украшения, предметы домашней утвари. Именно с открытием меди и других металлов стала зарождаться профессия кузнеца.
Позже появилось литьё, а потом человек стал добавлять к меди олово или сурьму, делать бронзу, более долговечную, прочную, легкоплавкую.
Сообщение 2 учащегося. Слайд 3
Бронза – сплав меди и олова. Хронологические границы бронзового века датируются в начале 3-го тысячелетия до н.э. до начала 1-го тысячелетия до н.э.
Сообщение 3 учащегося. Слайд 4
Третий и последний период первобытной эпохи характеризуется распространением железной металлургии и железных орудий и знаменует собой железный век. В современном значении этот термин был введен в употребление в середине IХ века датским археологом К. Ю. Томсоном и вскоре распространился в литературе наряду с терминами «каменный век» и « бронзовый век».
В отличие от других металлов железо, кроме метеоритного, почти не встречается в чистом виде. Ученые предполагают, что первое железо, попавшее в руки человека, было метеоритного происхождения, и не зря железо именуется « небесным камнем». Самый крупный метеорит нашли в Африке, он весил около шестидесяти тонн. А во льдах Гренландии нашли железный метеорит весом тридцать три тонны.
И настоящее время продолжается железный век. Ведь в настоящее время железные сплавы составляют почти 90 % всего металлов и металлических сплавов.
Учитель.
Золото и серебро – благородные металлы в настоящее время служат для изготовления ювелирных украшений, а также деталей в электронике, авиакосмической промышленности, в судостроении. Где в судоходстве могут применяться эти металлы? Исключительное значение металлов для развития общества обусловлено, конечно, их уникальными свойствами. Назовите эти свойства.
Продемонстрировать учащимся коллекцию образцов металлов.
Учащиеся называют такие свойства металлов как электропроводность и теплопроводность, характерный металлический блеск, пластичность, твердость (кроме ртути) и др.
Учитель задает учащимся ключевой вопрос: а чем же обусловлены эти свойства?
Ожидаемый ответ: свойства веществ обусловлены строением молекул и атомов этих веществ.
Слайд 5. Итак, металлы – группа веществ с общими свойствами.
Демонстрация презентации.
Учитель: Металлами являются элементы 1-3 групп главных подгрупп, и элементы 4-8 групп побочных подгрупп.
Слайд 6. Задание 1 . Самостоятельно, используя ПСХЭ, в тетради допишите представителей групп, являющиеся металлами.
VIII |
|||||||
Заслушивание ответов учащихся выборочно.
Учитель: металлами будут элементы, размещенные в левом нижнем углу ПСХЭ.
Учитель подчеркивает, что в ПСХЭ металлами будут все элементы, расположенные ниже диагонали В - Аt, даже те, у которых на внешнем слое 4 электрона (Gе, Sn, Рb), 5 электронов (Sb, Вi), 6 электронов (Ро), так как они отличаются большим радиусом.
Таким образом, из 109 элементов ПСХЭ 85 являются металлами. Слайд № 7
Учитель:
положение элемента в ПСХЭ отражает строение атома элемента. С помощью таблиц, которые вы получили в начале урока, охарактеризуем строение атома натрия по его положению в ПСХЭ.
Демонстрация слайда 8.
Что представляет собой атом натрия? Посмотрите на приближенную модель атома натрия, в которой видны ядро и электроны, движущиеся по орбитам.
Демонстрация Слайда 9. Модель атома натрия.
Напомню вам, как составляется схема электронного строения атома элемента.
Демонстрация слайда 10. У вас должна получиться следующая схема электронного строения атома натрия.
Слайд 11 . Задание 2. Составьте схему электронного строения атома кальция и алюминия в тетради самостоятельно по примеру с атомом натрия.
Учитель проверяет работу в тетради.
Какой вывод можно сделать об электронном строении атомов металлов?
На внешнем энергетическом уровне 1-3 электрона. Мы помним, что вступая в химические соединения, атомы стремятся восстановить полную 8-электронный оболочку внешнего энергетического уровня. Для этого атомы металлов легко отдают 1-3 электрона с внешнего уровня, превращаясь в положительно-заряженные ионы. При этом проявляют восстановительные свойства.
Демонстрация слайда 12. Металлы – это химические элементы, атомы которых отдают электроны внешнего (а иногда предвнешнего) электронного слоя, превращаясь в положительные ионы. Металлы – восстановители. Это обусловлено небольшим числом электронов внешнего слоя, большим радиусом атомов, вследствие чего эти электроны слабо удерживаются с ядром.
Рассмотрим простые вещества – металлы.
Демонстрация слайда 13.
Сначала обобщим сведения о типе химической связи, образуемой атомами металлов и строении кристаллической решетки
- сравнительно небольшое количество электронов одновременно связывают множество ядер, связь делокализована;
- валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален;
- металлическая связь не обладает направленностью и насыщенностью.
Демонстрация
Слайд 14 « Типы кристаллических решёток металлов »
Слайд 15 Видео кристаллической решетки металлов.
Учащиеся делают вывод, что в соответствие именно с таким строением металлы характеризуются общими физическими свойствами.
Учитель подчеркивает, что физические свойства металлов определяются именно их строением.
Слайд 16 Свойства металлов определяются строением их атомов
а) твердость – все металлы кроме ртути, при обычных условиях твердые вещества. Самые мягкие – натрий, калий. Их можно резать ножом; самый твердый хром – царапает стекло (демонстрация).
б) плотность - металлы делятся на лёгкие (5г/см) и тяжелые (больше 5г/см) (демонстрация).
в) плавкость - металлы делятся на легкоплавкие и тугоплавкие (демонстрация).
г) электропроводность, теплопроводность металлов обусловлена их строением. Хаотически движущиеся электроны под действием электрического напряжения приобретают направленное движение, в результате чего возникает электрический ток.
При повышении температуры амплитуда движения атомов и ионов, находящихся в узлах кристаллической решетки резко возрастает, и это мешает движению электронов, и электропроводность металлов падает.
Следует отметить, что у некоторых неметаллов, при повышении температуры электропроводность возрастает, например, у графита, при этом с повышением температуры разрушаются некоторые ковалентные связи, и число свободно перемещающихся электронов возрастает.
д) металлический блеск – электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают, как стекло.
Поэтому все металлы в кристаллическом состоянии имеют металлический блеск. Для большинства металлов в равной степени рассеиваются все лучи видимой части спектра, поэтому они имеют серебристо – белый цвет. Только золото и медь в большой степени поглощают короткие волны и отражают длинные волны светового спектра, поэтому имеют желтый свет. Самые блестящие металлы – ртуть, серебро, палладий. В порошке все металлы, кроме АI и Мg, теряют блеск и имеют черный или темно-серый цвет.
е) пластичность . Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и не сопровождается разрывом связи, и поэтому металл характеризуется высокой пластичностью.
IV. Закрепление изученного материала.
Учитель: мы рассмотрели строение и физические свойства металлов, их положение в периодической системе химических элементов Д.И. Менделеева. Теперь для закрепления предлагаем выполнить тест.
Слайды 15-16-17.
1) Электронная формула кальция.
- а) 1S 2 2S 2 2Р 6 3S 1
- б) 1S 2 2S 2 2Р 6 3S 2
- в) 1S 2 2S 2 2Р 6 3S 2 3S 6 4S 1
- г) 1S 2 2S 2 2Р 6 3S 2 3Р 6 4S 2
2) Электронную формулу 1S 2 2S 2 2Р 6 3S 2 3Р 6 4S 2 имеет атом:
- а) Nа
- б) Са
- в) Сu
- г) Zn
3) Электропроводность, металлический блеск, пластичность, плотность металлов определяются:
- а) массой металла
- б) температурой плавления металлов
- в) строением атомов металлов
- г) наличием неспареных электронов
4) Металлы при взаимодействии с неметаллами проявляют свойства
- а) окислительные;
- б) восстановительные;
- в) и окислительные, и восстановительные;
- г) не участвуют в окислительно-восстановительных реакциях;
5) В периодической системе типичные металлы расположены в:
- а) верхней части; VI. Домашнее задание.
- Диагональ В-Si-As-Те-At.
- Щелочные и щёлочноземельные металлы.
- Восстановительные свойства металлов.
- Относительность деления химических элементов на металлы и неметаллы.
Строение атомов металлов, их физические свойства
Как вам уже известно из курса химии 8 класса, большинство химических элементов относят к металлам (рис. 24 и 25).
Рис. 24.
Положение химических элементов-металлов в Периодической системе Д. И. Менделеева (короткопериодный вариант)
В Периодической системе Д. И. Менделеева каждый период, кроме первого (он включает в себя два элемента-неметалла - водород и гелий), начинается с активного химического элемента-металла. Эти элементы образуют главную подгруппу I группы (IA группу) и называются щелочными металлами. Своё название они получили от названия соответствующих им гидроксидов, хорошо растворимых в воде, - щелочей.

Рис. 25.
Положение химических элементов-металлов в Периодической системе Д. И. Менделеева (длиннопериодный вариант)
Атомы щелочных металлов содержат на внешнем энергетическом уровне только один электрон, который они легко отдают при химических взаимодействиях, поэтому являются сильнейшими восстановителями. Понятно, что в соответствии с увеличением радиуса атома восстановительные свойства щелочных металлов усиливаются от лития к францию.
Следующие за щелочными металлами элементы, составляющие главную подгруппу II группы (IIA группы), также являются типичными металлами, обладающими сильной восстановительной способностью (их атомы содержат на внешнем уровне два электрона). Из этих металлов кальций, стронций и барий называют щёлочноземельными металлами. Такое название эти металлы получили потому, что их оксиды, которые на Руси в старину называли «землями», при растворении в воде образуют щёлочи.
К металлам относят и химические элементы главной подгруппы III группы (IIIA группы), исключая бор.
Из элементов главных подгрупп следующих групп к металлам относят: в IVA группе - германий * , олово, свинец (первые два элемента - углерод и кремний - неметаллы), в VA группе - сурьму и висмут (первые три элемента - неметаллы), в VIA группе только последний элемент - полоний - явно выраженный металл. В главных подгруппах VIIA и VIIIA групп все элементы - типичные неметаллы.
-
* Германий проявляет и некоторые неметаллические свойства, занимая промежуточное положение между металлами и неметаллами.
Что касается элементов побочных подгрупп, то все они металлы.
Таким образом, условная граница между элементами-металлами и элементами-неметаллами проходит по диагонали В (бор) - Si (кремний) - As (мышьяк) - Те (теллур) - At (астат) (проследите её в таблице Д. И. Менделеева).
Атомы металлов имеют сравнительно большие размеры (радиусы), поэтому их внешние электроны значительно удалены от ядра и слабо с ним связаны. Вторая особенность, которая присуща атомам наиболее активных металлов, - это наличие на внешнем энергетическом уровне 1-3 электронов. Отсюда вытекает самое характерное химическое свойство всех металлов - их восстановительная способность, т. е. способность атомов легко отдавать внешние электроны, превращаясь в положительные ионы. Металлы - свободные атомы и простые вещества - не могут быть окислителями, т. е. атомы металлов не могут присоединять к себе электроны.
Следует, однако, иметь в виду, что деление химических элементов на металлы и неметаллы условно. Вспомните, например, свойства аллотропных модификаций олова: серое олово, или α-олово, - неметалл, а белое олово, или β-олово, - металл. Другой пример - модификации углерода: алмаз - неметалл, а графит имеет некоторые характерные свойства металла, например электропроводность. Хром, цинк и алюминий - типичные металлы, но образуют оксиды и гидроксиды амфотерного характера. И наоборот, теллур и иод - типичные неметаллы, но образованные ими простые вещества обладают некоторыми свойствами, присущими металлам.
Новые слова и понятия
Задания для самостоятельной работы
Металлы в периодической системе. Строение атомов-металлов. Общая характеристика металлов.
Положение металлов в периодической системе Если в таблице Д. И. Менделеева провести диагональ от бора к астату, то в главных подгруппах под диагональю окажутся атомы-металлы, а в побочных подгруппах все элементы ― металлы. Элементы, расположенные вблизи диагонали, обладают двойственными свойствами: в некоторых своих соединениях ведут себя как металлы; в некоторых ― как неметаллы.Строение атомов металлов В периодах и главных подгруппах действуют закономерности в изменении металлических свойств.Атомы многих металлов имеют 1, 2 или 3 валентных электрона, например:Na (+ 11): 1S 2 2S 2 2p 6 3S 1
Са (+ 20): 1S 2 2S 2 2p 6 3S 2 3p 6 3d 0 4S 2
Щелочные металлы (1 группа, главная подгруппа): ...nS 1 .Щелочно-земельные (2 группа, главная подгруппа): ...nS 2 .Свойства атомов–металлов находятся в периодической зависимости от их местоположения в таблице Д. И. Менделеева. В ГЛАВНОЙ ПОДГРУППЕ :
- не изменяется
.
Радиус атома увеличивается
Электроотрицательность уменьшается .
Восстановительные свойства усиливаются .
Металлические свойства усиливаются .
- Заряды ядер атомов увеличиваются
.
Радиусы атомов уменьшаются .
Число электронов на внешнем слое увеличивается .
Электроотрицательность увеличивается .
Восстановительные свойства уменьшаются .
Металлические свойства ослабевают .

а ― медь; б ― магний; в ― α-модификация железа
Атомы металлов стремятся отдать свои внешние электроны. В куске металла, слитке или металлическом изделии атомы металла отдают внешние электроны и посылают их в этот кусок, слиток или изделие, превращаясь при этом в ионы. «Оторвавшиеся» электроны перемещаются от одного иона к другому, временно снова соединяются с ними в атомы, снова отрываются, и этот процесс происходит непрерывно. Металлы имеют кристаллическую решетку, в узлах которой находятся атомы или ионы (+); между ними находятся свободные электроны (электронный газ). Схему связи в металле можно отобразить так:
М 0 ↔ nē + М n+ ,
атом ― ион
где n ― число внешних электронов, участвующих в связи (у Na ― 1 ē , у Са ― 2 ē , у Al ― 3 ē ).Наблюдается этот тип связи в металлах ― простых веществах-металлах и в сплавах.Металлическая связь ― это связь между положительно заряженными ионами металлов и свободными электронами в кристаллической решетке металлов.Металлическая связь имеет некоторое сходство с ковалентной, но и некоторое отличие, поскольку металлическая связь основана на обобществлении электронов (сходство), в обобществлении этих электронов принимают участие все атомы (отличие). Именно поэтому кристаллы с металлический связью пластичны, электропроводны и имеют металлический блеск. Однако в парообразном состоянии атомы металлов связаны между собой ковалентной связью, пары металлов состоят из отдельных молекул (одноатомных и двухатомных).Общая характеристика металлов
| Способность атомов отдавать электроны (окисляться) | ← Возрастает |
|||
| Взаимодействие с кислородом воздуха | Быстро окисляются при обычной температуре | Медленно окисляются при обычной температуре или при нагревании | Не окисляются |
|
| Взаимодействие с водой | При обычной температуре выделяется Н 2 и образуется гидроксид | При нагревании выделяется Н 2 | Н 2 из воды не вытесняют |
|
| Взаимодействие с кислотами | Вытесняют Н 2 из разбавленных кислот | Не вытесняют Н 2 из разбавленных кислот |
||
| Реагируют с конц. и разб. HNO 3 и с конц. H 2 SO 4 при нагревании | С кислотами не реагируют |
|||
| Нахождение в природе | Только в соединениях | В соединениях и в свободном виде | Главным образом в свободном виде |
|
| Способы получения | Электролиз расплавов | Восстановлением углем, оксидом углерода(2), алюмотермия, или электролиз водных растворов солей | ||
| Способность ионов присоединять электроны (восстанавливаться) | Li K Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb (H) Cu Hg Ag Pt Au |
|||
| Возрастает → |
||||
Электрохимический ряд напряжений металлов. Физические и химические свойства металлов
Общие физические свойства металлов Общие физические свойства металлов определяются металлической связью и металлической кристаллической решеткой. Ковкость, пластичность Механическое воздействие на кристалл металла вызывает смещение слоев атомов. Так как электроны в металле перемещаются по всему кристаллу, то разрыва связей не происходит. Пластичность уменьшается в ряду Au, Ag, Cu, Sn, Pb, Zn, Fe . Золото, например, можно прокатывать в листы толщиной не более 0,001 мм, которые используют для позолоты различных предметов. Алюминиевая фольга появилась сравнительно недавно и раньше чай, шоколад поковали в фольгу из олова, которая так и называлась ― станиоль. Однако не обладают пластичностью Mn и Bi: это хрупкие металлы. Металлический блеск Металлический блеск, который в порошке теряют все металлы, кроме Al и Mg . Самые блестящие металлы ― это Hg (из нее изготовляли в средние века знаменитые «венецианские зеркала»), Ag (из него теперь с помощью реакции «серебряного зеркала» изготовляют современные зеркала). По цвету (условно) различают металлы черные и цветные. Среди последних выделим драгоценные ― Au, Ag, Pt. Золото ― металл ювелиров. Именно на его основе изготовляли замечательные пасхальные яйца Фаберже. Звон Металлы звенят, и это свойство используется для изготовления колокольчиков (вспомните Царь-колокол в Московском Кремле). Самые звонкие металлы ― это Au, Ag, Cи. Медь звенит густым, гудящим звоном ― малиновым звоном. Это образное выражение не в честь ягоды-малины, а в честь голландского города Малина, где выплавлялись первые церковные колокола. В России потом русские мастера стали лить колокола даже лучшего качества, а жители городов и поселков жертвовали золотые и серебряные украшения, чтобы отливаемый для храмов колокол звучал лучше. В некоторых русских ломбардах определяли подлинность принимаемых на комиссию золотых колец по звону золотого обручального кольца, подвешенного на женском волосе (слышен очень долгий и чистый высокий звук). При нормальных условиях все металлы, кроме ртути Hg, ― твердые вещества. Самый твердый из металлов ― хром Cr: он царапает стекло. Самые мягкие ― щелочные металлы, они режутся ножом. Щелочные металлы хранят с большими предосторожностями ― Na ― в керосине, а Li ― в вазелине из-за своей легкости, керосин ― в стеклянной баночке, баночка ― в асбестовой крошке, асбест ― в жестяной баночке. Электропроводность Хорошая электрическая проводимость металлов объясняется присутствием в них свободных электронов, которые под влиянием даже небольшой разности потенциалов приобретают направленное движение от отрицательного полюса к положительному. С повышением температуры усиливаются колебания атомов (ионов), что затрудняет направленное движение электронов и тем самым приводит к уменьшению электрической проводимости. При низких же температурах колебательное движение, наоборот, сильно уменьшается и электрическая проводимость резко возрастает. Вблизи абсолютного нуля металлы проявляют сверхпроводимость. Наибольшей электрической проводимостью обладают Ag, Cu, Au, Al, Fe; худшие проводники ― Hg, Pb, W. Теплопроводность При обычных условиях теплопроводность металлов изменяется в основном в такой же последовательности, как их электрическая проводимость. Теплопроводность обусловливается высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры в массе металла. Наибольшая теплопроводность ― у серебра и меди, наименьшая ― у висмута и ртути. Плотность Плотность металлов различна. Она тем меньше, чем меньше атомная масса элемента-металла и чем больше радиус его атома. Самый легкий из металлов ― литий (плотность 0,53 г/см 3), самый тяжелый ― осмий (плотность 22,6 г/см 3). Металлы с плотностью меньше 5 г/см 3 называются легкими, остальные ― тяжелыми. Разнообразны температуры плавления и кипения металлов. Самый легкоплавкий металл ― ртуть (t кип = -38,9°С), цезий и галлий ― плавятся соответственно при 29 и 29,8°С. Вольфрам ― самый тугоплавкий металл (t кип = 3390°С). Понятие аллотропии металлов на примере олова Некоторые металлы имеют аллотропные модификации. Например, олово различают на:- α-олово, или серое олово («оловянная чума» ― превращение обычного β-олова в α-олово при низких температурах стало причиной гибели экспедиции Р. Скотта к Южному полюсу, который потерял все горючее, так как оно хранилось в баках, запаянных оловом), устойчиво при t <14°С, серый порошок. β-олово, или белое олово (t = 14 ― 161°С) очень мягкий металл, но тверже свинца, поддается литью и пайке. Используется в сплавах, например, для изготовления белой жести (луженого железа).
- С галогенами металлы образуют соли ― галогениды:
- С кислородом металлы образуют оксиды:
- С серой металлы образуют соли ― сульфиды:
- С водородом самые активные металлы образуют гидриды, например:
- с углеродом многие металлы образуют карбиды:
- Металлы, находящиеся в начале ряда напряжений (от лития до натрия), при обычных условиях вытесняют водород из воды и образуют щелочи, например:
- Металлы, расположенные в ряду напряжений до водорода, взаимодействуют с разбавленными кислотами (НCl, Н 2 SO 4 и др.), в результате чего образуются соли и выделяется водород, например:
- Металлы взаимодействуют с растворами солей менее активных металлов, в результате чего образуется соль более активного металла, а мене активный металл выделяется в свободном виде, например:
Металлы в природе.
Нахождение металлов в природе. Большинство металлов встречается в природе в виде различных соединений: активные металлы находятся только в виде соединений; малоактивные металлы ― в виде соединений и в свободном виде; благородные металлы (Аg, Рt, Аu...) в свободном виде.Самородные металлы обычно содержатся в небольших количествах в виде зерен или вкраплений в горных породах. Изредка встречаются и довольно крупные куски металлов ― самородки. Многие металлы в природе существуют в связанном состоянии в виде химических природных соединений ― минералов . Очень часто это оксиды, например минералы железа: красный железняк Fe 2 O 3 , бурый железняк 2Fe 2 O 3 ∙ 3Н 2 О, магнитный железняк Fe 3 O 4 .Минералы входят в состав горных пород и руд. Рудами называют содержащие минералы природные образования, в которых металлы находятся в количествах, пригодных в технологическом и экономическом отношении для получения металлов в промышленности.По химическому составу минерала, входящего в руду, различают оксидные, сульфидные и другие руды.Обычно перед получением металлов из руды ее предварительно обогащают ― отделяют пустую горную породу, примеси, в результате образуется концентрат, служащий сырьем для металлургического производства.Способы получения металлов. Получение металлов из их соединений ― это задача металлургии. Любой металлургический процесс является процессом восстановления ионов металла с помощью различных восстановителей, в результате чего получаются металлы в свободном виде. В зависимости от способа проведения металлургического процесса различают пирометаллургию, гидрометаллургию и электрометаллургию.Пирометаллургия ― это получение металлов из их соединений при высоких температурах с помощью различных восстановителей: углерода, оксида углерода (II), водорода, металлов (алюминия, магния) и др.Примеры восстановления металлов- углем:
- оксидом углерода:
- водородом:
- алюминием (алюмотермия):
- магнием:
- 2CuS + 3О 2 = 2CuO + 2SО 2 .
- CuSO 4 + Fe = FeSO 4 + Cu.
Общая характеристика металлов IА-группы.
К металлам главной подгруппы первой группы (IА-группы) относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs), франций (Fr). Эти металлы называются щелочными, так как они и их оксиды при взаимодействии с водой образуют щелочи.Щелочные металлы относятся к s-элементам. На внешнем электронном слое у атомов металлов один s-электрон (ns 1).Калий, натрий ― простые вещества

Щелочные металлы в ампулах:
а - цезий; б - рубидий; в - калий; г – натрийОсновные сведения об элементах IА группы
| Элемент | Li литий | Na натрий | K калий | Rb рубидий | Cs цезий | Fr франций |
| Атомный номер | 3 | 11 | 19 | 37 | 55 | 87 |
| Строение внешних электрон-ных оболочек атомов | ns 1 np 0 ,где n = 2, 3, 4, 5, 6, 7, n ― номер периода | |||||
| Степень окисления | +1 | +1 | +1 | +1 | +1 | +1 |
| Основные природные соединения | Li 2 O·Al 2 O 3 · 4SiO 2 (сподумен); LiAl(PO 4)F, LiAl(PO 4)OH (амблигонит) | NaCl (поварен-ная соль); Na 2 SO 4 · 10H 2 O (глауберо-ва соль, мираби-лит); КCl·NaCl (сильви-нит) | КCl (сильвин), КCl·NaCl (сильвинит); K (калиевый полевой шпат, ортоглаз); KCl·MgCl 2 ·6H 2 O (карналлит) ― содержится в растениях | В качестве изоаморф-ной примеси в минералах калия ― сильвини-те и кар-наллите | 4Cs 2 O·4Al 2 O 3 ·18 SiO 2 · 2H 2 O (полу-цит); спутник минера-лов калия | Продукт α-распада актиния |
Положение металлов
в периодической системе химических элементов
Д.И.Менделеева.
Физические свойства металлов
8 класс
Цель. Дать учащимся представление о свойствах металлов как химических элементов и как простых веществ, опираясь на их знания о природе химической связи. Рассмотреть применение простых веществ-металлов на основе их свойств. Совершенствовать умение сравнивать, обобщать, устанавливать взаимосвязь строения и свойств веществ. Развивать познавательную активность учеников, применяя игровые формы учебной деятельности.
Оборудование и реактивы. Карточки-задания, карточки с символами щелочных металлов (на каждого ученика), планшеты, таблица «Металлическая связь», игры «Алхимические знаки», спиртовка, старые медные монеты, батистовый мешочек, образцы металлов.
ХОД УРОКА
Учитель. Сегодня мы изучим металлы как химические элементы и металлы как простые вещества. Что называется химическим элементом?
Ученик. Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
Учитель. Из 114 известных химических элементов 92 – металлы. Где в периодической системе химических элементов расположены металлы? Как расположены элементы-металлы в периодах?
Работа по таблице «Периодическая система химических элементов Д.И.Менделеева».
Ученик. Металлами начинается каждый период (кроме первого), и число их возрастает с увеличением номера периода.
Учитель. Сколько элементов-металлов в каждом периоде?
Статья подготовлена при поддержке школы английского языка в Москве «Аллада». Знание английского языка позволяет расширить свой кругозор, а также вы сможете познакомиться с новыми людьми и узнать много нового. Школа английского языка «Аллада» предоставляет уникальную возможность записать на курсы английского языка по оптимальной цене. Более подробную информацию о ценах и акциях действующих на данный момент вы сможете найти на сайте www.allada.org.
Ученик. В первом периоде металлов нет, во втором их два, в третьем – три, в четвертом – четырнадцать, в пятом – пятнадцать, в шестом – тридцать.
Учитель. В седьмом периоде свойствами металла должен обладать тридцать один элемент. Давайте посмотрим расположение металлов в группах.
Ученик. Металлы – это элементы, составляющие главные подгруппы I, II, III групп периодической системы (за исключением водорода и бора), элементы IV группы – германий, олово, свинец, V группы – сурьма, висмут, VI группы – полоний. В побочных подгруппах всех групп находятся только металлы.
Учитель. Элементы-металлы расположены в левой и нижней части периодической системы. А сейчас сделайте в тетрадях задание 1 из карточки-задания.
Задание 1. Выпишите из карточек химические знаки металлов. Назовите их. Подчеркните металлы главных подгрупп.
1-й в а р и а н т. Na, В, Сu, Be, Se, F, Sr, Cs.
О т в е т. Na
– натрий
, Сu
–
медь
,
Be
– бериллий
, Sr
– стронций
, Cs
–
цезий.
2-й в а р и а н т. K, С, Fe, Mg, Ca, О, N, Rb.
О т в е т. K
– калий
, Fe
– железо
,
Mg
– магний
, Ca
– кальций
, Rb
–
рубидий
.
Учитель. Каковы особенности строения атомов металлов? Составьте электронные формулы атомов натрия, магния, алюминия.
(У доски работают три ученика, используя рисунок (рис. 1).)
Сколько электронов на внешнем уровне этих элементов-металлов?
Ученик. Число электронов на внешнем уровне у элементов главных подгрупп равно номеру группы, у натрия на внешнем уровне один электрон, у магния – два электрона, у алюминия – три электрона.
Учитель. Атомы металлов имеют малое число электронов (в основном от 1 до 3) на внешнем уровне. Исключение составляют шесть металлов: атомы германия, олова и свинца на внешнем слое имеют 4 электрона, атомы сурьмы, висмута – 5, атомы полония – 6. А теперь сделайте второе задание из карточки.
Задание 2. Приведены схемы электронного строения атомов некоторых элементов.
Какие это элементы? Какие из них принадлежат к металлам? Почему?
1-й в а р и а н т. 1s 2 , 1s 2 2s 2 , 1s 2 2s 2 2p 6 3s 2 , 1s 2 2s 2 2p 3 .
О т в е т. Гелий, бериллий, магний, азот.
2-й вариант. 1s 2 2s 1 , 1s 2 2s 2 2p 6 3s 1 , 1s 1 , 1s 2 2s 2 2p 6 3s 2 3p l .
О т в е т. Литий, натрий, водород, алюминий.
Учитель. Как связаны свойства металлов с особенностями их электронного строения?
Ученик. Атомы металлов имеют меньший заряд ядра и больший радиус по сравнению с атомами неметаллов того же периода. Поэтому прочность связи внешних электронов с ядром в атомах металлов небольшая. Атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы.
Учитель. Как изменяются металлические свойства в пределах одного и того же периода, одной и той же группы (главной подгруппы)?
Ученик. В пределах периода с ростом заряда атомного ядра, а соответственно и с ростом числа внешних электронов металлические свойства химических элементов уменьшаются. В пределах одной и той же подгруппы с ростом заряда атомного ядра, при постоянном числе электронов на внешнем уровне металлические свойства химических элементов увеличиваются.
Задание у доски (работают три ученика).
Указать знаком «» ослабление металлических свойств в следующих пятерках элементов. Объяснить расстановку знаков.
| 1. | Be | 2. | Mg | 3. | Al | |||
| Na | Mg | Al | K | Ca | Sc | Zn | Ga | Ge |
| Ca | Sr | In |
Пока учащиеся работают индивидуально у доски, остальные выполняют задание 3 из карточки.
Задание 3. Какой из двух элементов обладает более выраженными металлическими свойствами? Почему?
1-й в а р и а н т. Литий или бериллий.
2-й в а р и а н т. Литий или калий.
Проверка заданий.
Учитель. Итак, металлическими свойствами обладают те элементы, атомы которых имеют мало электронов на внешнем уровне (далеком до завершения). Следствие небольшого числа внешних электронов – слабая связь этих электронов с остальной частью атома – ядром, окруженным внутренними слоями электронов.
Подводится итог и записывается кратко на доске (схема), ученики записывают в тетрадях.
Схема
Учитель. Что называется простым веществом?
Ученик. Простые вещества – это вещества, которые состоят из атомов одного элемента.
Учитель. Простые вещества-металлы – это «коллективы» атомов; в силу электронейтральности каждого атома вся масса металла тоже электронейтральна, что позволяет брать в руки металлы, рассматривать их.
Демонстрация образцов металлов: никель, золото, магний, натрий (в склянке под слоем керосина).
А вот натрий голыми руками брать нельзя – руки влажные, при взаимодействии с влагой образуется щелочь, а она разъедает кожу, ткани, бумагу и другие материалы. Так что последствия для руки могут быть печальными.
Задание 4. Определите металлы из числа выданных: свинец, алюминий, медь, цинк.
(Образцы металлов пронумерованы. Ответы записаны на обратной стороне доски.)
Проверка задания.
Учитель. В каком агрегатном состоянии при обычных условиях находятся металлы?
Ученик. Металлы – это твердые кристаллические вещества (кроме ртути).
Учитель. Что находится в узлах кристаллической решетки металлов и что между узлами?
Ученик. В узлах кристаллической решетки металлов находятся положительные ионы и атомы металлов, между узлами – электроны. Эти электроны становятся общими для всех атомов и ионов данного куска металла и могут свободно перемещаться по всей кристаллической решетке.
Учитель. Как называют электроны, которые находятся в кристаллической решетке металлов?
Ученик. Их называют свободными электронами или «электронным газом».
Учитель. Какой тип связи характерен для металлов?
Ученик. Это металлическая связь.
Учитель. Что называется металлической связью?
Ученик. Связь между всеми положительно заряженными ионами металлов и свободными электронами в кристаллической решетке металлов называется металлической связью.
Учитель. Металлическая связь обуславливает важнейшие физические свойства металлов. Металлы непрозрачны, обладают металлическим блеском, обусловленным способностью отражать падающие на их поверхность световые лучи. В наибольшей степени эта способность проявляется у серебра и индия.
Металлы имеют блеск в компактном куске, а в мелкодисперсном состоянии большинство из них черного цвета. Однако алюминий, магний сохраняют металлический блеск даже в порошкообразном состоянии (демонстрация алюминия и магния в порошке и в пластинках).
Все металлы – проводники теплоты и электрического тока. Хаотически движущиеся электроны в металле под воздействием приложенного электрического напряжения приобретают направленное движение, т.е. создают электрический ток.
Как вы думаете, изменяется ли электрическая проводимость металла при повышении температуры?
Ученик. С повышением температуры электропроводность снижается.
Учитель. Почему?
Ученик. При повышении температуры возрастает амплитуда колебаний атомов и ионов, находящихся в узлах кристаллической решетки металла. Это затрудняет перемещение электронов, и электрическая проводимость металла падает.
Учитель. Электропроводность металлов возрастает от Hg к Ag:
Hg, Pb, Fe, Zn, Al, Au, Cu, Ag.
Чаще всего с той же закономерностью, как и электрическая проводимость, изменяется теплопроводность металлов. Можете ли вы привести пример, доказывающий теплопроводность металлов?
Ученик. Если в алюминиевую кружку налить горячую воду, она нагреется. Это свидетельствует о том, что алюминий проводит теплоту.
Учитель. Чем обусловлена теплопроводность металлов?
Ученик. Она обусловлена большой подвижностью свободных электронов, которые сталкиваются с колеблющимися ионами и атомами, обмениваются с ними энергией. Поэтому происходит выравнивание температуры по всему куску металла.
Учитель. Весьма ценным свойством металлов является пластичность. На практике она проявляется в том, что под ударами молота металлы не дробятся на куски, а расплющиваются – они ковки. Почему металлы пластичны?
Ученик. Механическое воздействие на кристалл с металлической связью вызывает смещение слоев ионов и атомов относительно друг друга, а т.к. электроны перемещаются по всему кристаллу, разрыва связи не происходит, поэтому для металлов характерна пластичность (рис. 2, а).
Учитель. Ковкие металлы: щелочные металлы (литий, натрий, калий, рубидий, цезий), железо, золото, серебро, медь. Некоторые металлы – осмий, иридий, марганец, сурьма – хрупкие. Самым пластичным из драгоценных металлов является золото. Один грамм золота можно вытянуть в проволоку длиной в два километра.
А что происходит под действием удара с веществами с атомной или ионной кристаллической решеткой?
Ученик. Вещества с атомной или ионной решеткой под действием удара разрушаются. При механическом воздействии на твердое вещество с атомной решеткой смещаются отдельные ее слои – сцепление между ними нарушается из-за разрыва ковалентных связей. Разрыв связей в ионной решетке приводит к взаимному отталкиванию одноименно заряженных ионов (рис. 2, б, в).
Учитель. Электропроводность, теплопроводность, характерный металлический блеск, пластичность, или ковкость, – такая совокупность признаков присуща только металлам. Эти признаки проявляются в металлах и являются специфическими свойствами.
Специфические свойства находятся в обратной зависимости от прочности металлической связи. Остальные свойства – плотность, температуры кипения и плавления, твердость, агрегатное состояние – общие, присущие всем веществам признаки.
Плотность, твердость, температуры плавления и кипения металлов различны. Плотность металла тем меньше, чем меньше его относительная атомная масса и чем больше радиус атома. Наименьшая плотность у лития – 0,59 г/см 3 , наибольшая у осмия – 22,48 г/см 3 . Металлы, плотность которых ниже пяти, называют легкими, а металлы с плотностью больше пяти – тяжелыми.
Самый твердый металл – хром, самые мягкие – щелочные металлы.
Самую низкую температуру плавления имеет ртуть, t пл (Hg) = –39 °С, а самую высокую – вольфрам, t пл (W) = 3410 °С.
Такие свойства, как температура плавления, твердость, находятся в прямой зависимости от прочности металлической связи. Чем прочнее металлическая связь, тем жестче неспецифические свойства. Обратите внимание: у щелочных металлов прочность металлической связи уменьшается в периодической таблице сверху вниз и, как следствие, закономерно уменьшается температура плавления (растет радиус, влияние заряда ядра уменьшается, при больших радиусах и единственном валентном электроне щелочные металлы легкоплавки). Например, цезий можно расплавить теплом ладони. Но не стоит брать его голой рукой!
Игра «Кто быстрее»
На доске вывешиваются планшеты (рис. 3). На каждой парте набор карточек с химическими знаками щелочных металлов.
Задание. Опираясь на известные закономерности изменения температуры плавления щелочных металлов, разместить карточки в соответствии с данными планшетами.
О т в е т. a
– Li, Na, K, Rb, Cs;
б
– Cs, Rb, K, Na, Li; в
– Cs, Li, Na, Rb, K.
Уточняются и обобщаются ответы учащихся.
Ученик (cообщение). Металлы различаются своим отношением к магнитным полям. По этому свойству их делят на три группы: ферромагнитные металлы – способные хорошо намагничиваться при действии слабых магнитных полей (например, железо, кобальт, никель и гадолиний); парамагнитные металлы – проявляющие слабую способность к намагничиванию (алюминий, хром, титан и большая часть лантаноидов); диамагнитные металлы – не притягивающиеся к магниту и даже слегка отталкивающиеся от него (например, висмут, олово, медь).
Обобщается изученный материал – учитель записывает на доске, учащиеся пишут в тетрадях.
Физические свойства металлов
Специфические:
металлический блеск,
электропроводность,
теплопроводность,
пластичность.
Обратно пропорциональная зависимость от прочности металлической связи.
Неспецифические: плотность,
t плавления,
t кипения,
твердость,
агрегатное состояние.
Прямо пропорциональная зависимость от прочности металлической связи.
Учитель. Физические свойства металлов, вытекающие из свойств металлической связи, обуславливают их разнообразное применение. Металлы и их сплавы – важнейшие конструкционные материалы современной техники; они идут на изготовление машин и станков, необходимых в промышленности, различных транспортных средств, строительных конструкций, сельскохозяйственных машин. В связи с этим сплавы железа, алюминия производят в больших количествах. Металлы широко применяются в электротехнике. Из каких металлов делают электрические провода?
Ученик. В электротехнике из-за дороговизны серебра в качестве материала для электропроводки используют медь и алюминий .
Учитель. Без этих металлов невозможно было бы передать электрическую энергию на расстояние в сотни, тысячи километров. Предметы быта также изготовлены из металлов. Почему кастрюли делают из металлов?
Ученик. Металлы теплопроводны и прочны.
Учитель. Какое свойство металлов используют для изготовления зеркал, рефлекторов, елочных игрушек?
Ученик. Металлический блеск.
Учитель. Легкие металлы – магний, алюминий, титан – широко используют в самолетостроении. Из титана и его сплавов изготавливают многие детали самолетов, ракет. Трение о воздух при больших скоростях вызывает сильное разогревание обшивки самолета, а прочность металлов при нагреве обычно значительно снижается. У титана и его сплавов в условиях сверхзвуковых полетов снижение прочности почти не наблюдается.
В тех случаях, когда необходим металл с большой плотностью (пули, дробь), часто используют свинец, хотя плотность свинца (11,34 г/см 3) значительно ниже, чем некоторых более тяжелых металлов. Но свинец довольно легкоплавок и поэтому удобен при обработке. К тому же он несравнимо дешевле осмия и многих других тяжелых металлов. Ртуть, как жидкий при обычных условиях металл, применяют в измерительных приборах; вольфрам – во всех случаях, когда требуется металл, противостоящий особенно высоким температурам, например для нитей накаливания электролампочек. Чем это обусловлено?
Ученик. У ртути – низкая температура плавления, а у вольфрама – высокая.
Учитель. Металлы также отражают радиоволны, что используется в радиотелескопах, улавливающих радиоизлучение искусственных спутников Земли, и в радиолокаторах, обнаруживающих самолеты на больших расстояниях.
Благородные металлы – серебро, золото, платина – используются для изготовления украшений. Потребителем золота является электронная отрасль промышленности: оно используется для изготовления электрических контактов (в частности, аппаратура пилотируемого космического корабля содержит достаточно много золота).
А теперь сделайте задание из карточки.
Задание 5. Подчеркнуть, какой из приведенных металлов самый:
1) широко используемый: золото, серебро, железо;
2) ковкий: литий, калий, золото;
3) тугоплавкий: вольфрам, магний, цинк;
4) тяжелый: рубидий, осмий, цезий;
5) электропроводный: никель, свинец, серебро;
6) твердый: хром, марганец, медь;
7) легкоплавкий: платина, ртуть, литий;
8) легкий: калий, франций, литий;
9) блестящий: калий, золото, серебро.
Демонстрация опыта
Для опыта берется 5–10 штук медных (старых) монет, которые подвешивают в батистовом мешочке над пламенем спиртовки. Ткань не загорается. Почему?
Ученик. Медь хороший проводник тепла, тепло сразу передается металлу, и ткань не успевает загореться.
Учитель. Металлы известны человеку давно.
Ученик (сообщение). Еще в глубокой древности человеку были известны семь металлов. Семь металлов древности соотносили с семью известными тогда планетами и обозначали символическими значками планет. Знаки золота (Солнца) и серебра (Луны) понятны без особых пояснений. Знаки же других металлов считались атрибутами мифологических божеств: ручное зеркало Венеры (медь), щит и копье Марса (железо), трон Юпитера (олово), коса Сатурна (свинец), жезл Меркурия (ртуть).
Взгляды алхимиков о связи планет с металлами очень удачно выражают следующие строки стихотворения Н.А.Морозова «Из записок алхимика»:
«Семь металлов создал свет,
По числу семи планет.
Дал нам космос на добро
Медь, железо, серебро,
Злато, олово, свинец.
Сын мой, сера – их отец.
И спеши, мой сын, узнать:
Всем им ртуть – родная мать».
Эти представления были настолько прочными,
что, когда для открытых в средние века сурьмы
и висмута не нашлось планет, их просто не
посчитали металлами.
Держа свои опыты в тайне, алхимики всевозможными способами зашифровывали описания полученных веществ.
Учитель. И вы, используя алхимические обозначения, дома составили игру «Алхимические знаки».
Условие игры: на рисунке (рис. 4) приведены древние алхимические знаки металлов. Определите, какой планете принадлежит каждый символ и, взяв из названия по одной букве, той, что указаны на рисунке, прочтите название элемента-металла.
О т в е т ы. Самарий, рутений, платина.
Учащиеся обмениваются играми, отгадывают названия металлов.
Учитель. М.В.Ломоносов так говорил о металлах: «Металлом называется твердое, непрозрачное и светлое тело, которое на огне плавить и холодное ковать можно» и относил это свойство к металлам: золоту, серебру, меди, олову, железу и свинцу.
В 1789 г. французский химик А.Л.Лавуазье в своем руководстве по химии дал список простых веществ, в который включил все известные тогда 17 металлов (Sb, Ag, As, Bi, Co, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn). По мере развития методов химического исследования число известных металлов стало быстро возрастать. В первой половине XIX в. были открыты платиновые металлы; получены путем электролиза некоторые щелочные и щелочно-земельные металлы; положено начало разделению редкоземельных металлов; при химическом анализе минералов открыты неизвестные ранее металлы. В начале 1860 г. с помощью спектрального анализа были открыты рубидий, цезий, индий, таллий. Блестяще подтвердилось существование металлов, предсказанных Менделеевым на основе его периодического закона (галлия, скандия и германия). Открытие радиоактивности в конце XIX в. повлекло за собой поиски радиоактивных металлов, увенчавшиеся полным успехом. Наконец, методом ядерных превращений, начиная с середины XX в. были получены не существующие в природе радиоактивные металлы, в том числе и те, что принадлежат к трансурановым элементам. В истории материальной культуры, древней и новой, металлы имеют первостепенное значение.
Учитель подводит итог урока.
Домашнее задание
1. Найдите ответы на вопросы.
Чем отличается строение атомов металлов от строения атомов неметаллов?
Назовите два металла, легко расстающихся с электронами по «просьбе» световых лучей.
Можно ли принести в кабинет химии из соседнего кабинета ведро ртути?
Почему некоторые металлы пластичные (например, медь), а другие – хрупкие (например, сурьма)?
В чем причина присутствия у металлов специфических свойств?
Где можно встретить в быту:
а) вольфрам, б) ртуть, в) медь, г) серебро?
На каких физических свойствах данного металла основано применение его в быту?
Какой металл академик А.Е.Ферсман назвал «металлом консервной банки»?
2. Посмотрите на рисунок и объясните, почему металлы использованы именно таким образом, а не наоборот.

3. Решите головоломки.
Головоломка «Пять + два».
Впишите в горизонтальные ряды названия следующих химических элементов, оканчивающихся на -ий:
а) щелочной металл;
б) благородный газ;
в) щелочно-земельный металл;
г) элемент семейства платины;
д) лантаноид.

Если названия элементов будут вписаны правильно, то по диагоналям: сверху вниз и снизу вверх можно будет прочесть названия еще двух элементов.
О т в е т ы. а – Цезий, б – гелий,
в – барий, г – родий, д – тулий.
По диагонали: церий, торий.
Головоломка «Класс».

Впишите названия пяти химических элементов, состоящие из семи букв каждое, таким образом, чтобы ключевое слово было КЛАСС.
О т в е т ы. Кальций (кобальт), лютеций,
актиний, скандий, серебро (самарий).
Головоломка «Семь букв».
Впишите названия химических элементов в вертикальные ряды.
Ключевое слово – КИСЛОТА.

О т в е т ы. Калий, индий, селен, литий,
осмий, тулий, аргон (астат).
Положение металлов в периодической системе. Физические свойства
В периодической системе Д. И. Менделеева из 110 элементов 87 являются металлами. Они находятся в I, II, III группах, в побочных подгруппах всех групп. Кроме того, металлами являются наиболее тяжелые элементы IV, V, VI и VII групп. Однако многие металлы обладают амфотерными свойствами и иногда могут вести себя как неметаллы. Особенностью строения атомов металлов является небольшое число электронов во внешнем энергетическом уровне, не превышающее трех. Атомы металлов имеют, как правило, большие атомные радиусы. В периодах наибольшие атомные радиусы у щелочных металлов. Они наиболее химически активны, т.е. атомы металлов легко отдают электроны и являются хорошими восстановителями. Лучшие восстановители - металлы I и II групп главных подгрупп. В соединениях металлы всегда проявляют положительную степень окисления, обычно от +1 до +4. В соединениях с неметаллами типичные металлы образуют химическую связь ионного характера. В виде простого вещества атомы металлов связаны между собой так называемой металлической связью.
Металлическая связь - особый вид связи, присущий исключительно металлам. Сущность ее в том, что от атомов металла постоянно отрываются электроны, которые перемещаются по всей массе куска металла.
Атомы металла, лишенные электронов, превращаются в положительные ионы, которые снова притягивают к себе движущиеся электроны. Одновременно другие атомы металла отдают электроны. Таким образом, внутри куска металла постоянно циркулирует так называемый электронный газ, который прочно связывает между собой все атомы металла. Электроны оказываются как бы обобществленными всеми атомами металла. Такой особый тип химической связи между атомами металлов обуславливает как физические, так и химические свойства металлов.
Металлы обладают рядом сходных физических свойств, отличающих их от неметаллов. Чем больше валентных электронов имеет металл, тем прочнее кристаллическая решетка, тем прочнее и тверже металл, тем выше его температура плавления и кипения и т.д.
Все металлы обладают более или менее ярко выраженным блеском, который принято называть металлическим, и непрозрачностью, что связано с взаимодействием свободных электронов с падающими на металл квантами света. Металлический блеск характерен для куска металла в целом. В порошке металлы темного цвета, за исключением серебристо-белых магния и алюминия. Алюминиевая пыль используется для изготовления краски «под серебро». Многие металлы обладают жирным или стеклянным блеском.
Цвет металлов довольно однообразен: он либо серебристо-белый (алюминий, серебро, никель), либо серебристо-серый (железо, свинец). Только золото желтого цвета, а медь - красного. По технической классификации металлы делятся условно на черные и цветные. К черным относятся железо и его сплавы. Все остальные металлы называются цветными.
Все металлы, за исключением ртути, - твердые вещества с кристаллической структурой, поэтому температуры плавления их выше нуля, только температура плавления ртути - З9°C. Наиболее тугоплавким металлом является вольфрам (3380°С). Металлы, плавящиеся при температуре выше 1000°С, называют тугоплавкими, ниже - легкоплавкими.
Металлы обладают различной твердостью. Самый твердый металл - хром (режет стекло), а самые мягкие - калий, рубидий, цезий. Они легко режутся ножом.
Металлы более или менее пластичны (обладают ковкостью). Наиболее ковким металлом является золото. Из него можно выковать фольгу толщиной 0,0001 мм - в 500 раз тоньше человеческого волоса. Однако не обладают пластичностью Mn и Bi - это хрупкие металлы.
Пластичностью называют способность к сильной деформации без нарушения механической прочности. При воздействии, вызывающем смещение частиц тела с ионной или атомной решеткой, происходит разрыв направленных связей, и тело разрушается. У металлов же связи образуются за счет электронного газа. Они не имеют направленности. Поэтому сохраняется целостность куска металла при изменении формы. Пластичность металлов используется при их прокате.
По плотности металлы разделяются на тяжелые и легкие. Тяжелыми считаются те, плотность которых больше 5 г/см. Самым тяжелым металлом является осмий (22,61 г/см). Наиболее легкие металлы - литий, натрий, калий (плотность меньше единицы). Плотность металла тем меньше, чем меньше атомная масса элемента-металла и чем больше радиус его атома. Широкое применение в промышленности получили легкие металлы - магний и алюминий.
Металлы характеризуются высокой электро- и теплопроводностью. Наиболее электро- и теплопроводно серебро, на втором месте стоит алюминий. Металлы с высокой электропроводностью имеют и высокую теплопроводность. Теплопроводность обуславливается высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры в массе тела. Хорошая электропроводность металлов объясняется присутствием в них свободных электронов, которые под влиянием даже небольшой разницы потенциалов приобретают направленное движение от отрицательного полюса к положительному.
Металлы проявляют магнитные свойства. Хорошо намагничиваются железо, кобальт, никель и их сплавы. Такие металлы и сплавы называются ферромагнитными.