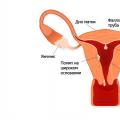
Твердыми называют такие вещества, которые способны образовывать тела и имеют объем. От жидкостей и газов они отличаются своей формой. Твердые вещества сохраняют форму тела благодаря тому, что их частицы не способны свободно перемещаться. Они отличаются по своей плотности, пластичности, электропроводности и цвету. Также у них есть и другие свойства. Так, например, большинство данных веществ плавятся во время нагревания, приобретая жидкое агрегатное состояние. Некоторые из них при подогреве сразу же превращаются в газ (возгоняются). Но есть еще и те, которые разлагаются на иные вещества.
Виды твердых веществ
Все твердые вещества подразделяют на две группы.
- Аморфные, в которых отдельные частицы располагаются хаотично. Другими словами: в них нет четкой (определенной) структуры. Эти твердые вещества способны плавиться в каком-то установленном промежутке температур. К самым распространенным из них можно отнести стекло и смолу.
- Кристаллические, которые, в свою очередь, подразделяются на 4 типа: атомные, молекулярные, ионные, металлические. В них частицы располагаются только по определенной схеме, а именно в узлах кристаллической решетки. Ее геометрия в разных веществах может сильно различаться.
Твердые кристаллические вещества преобладают над аморфными по своей численности.
Типы кристаллических твердых веществ
В твердом состоянии практически все вещества имеют кристаллическую структуру. Они отличаются своим решетки в своих узлах содержат различные частицы и химические элементы. Именно в соответствии с ними они и получили свои названия. У каждого типа имеются характерные для него свойства:
- В атомной кристаллической решетке частицы твердого вещества связаны ковалентной связью. Она отличается своей прочностью. Благодаря этому такие вещества отличаются высокой и кипения. К этому типу относятся кварц и алмаз.
- В молекулярной кристаллической решетке связь между частицами отличается своей слабостью. Вещества такого типа характеризуются легкостью закипания и плавления. Они отличаются летучестью, благодаря которой имеют определенный запах. К таким твердым телам относятся лед, сахар. Движения молекул в твердых веществах этого типа отличаются своей активностью.
- В в узлах чередуются соответствующие частицы, заряженные положительно и отрицательно. Они удерживаются электростатическим притяжением. Данный тип решетки существует в щелочах, солях, Многие вещества этого вида легко растворяются в воде. Благодаря достаточно прочной связи между ионами они тугоплавки. Практически все они не имеют запаха, поскольку для них характерна нелетучесть. Вещества с ионной решеткой неспособны проводить электрический ток, поскольку в их составе нет свободных электронов. Типичный пример ионного твердого вещества - поваренная соль. Такая кристаллическая решетка придает ей хрупкость. Это связано с тем, что любой ее сдвиг может привести к возникновению сил отталкивания ионов.
- В металлической кристаллической решетке в узлах присутствуют только ионы химических веществ, заряженные положительно. Между ними есть свободные электроны, через которые отлично проходит тепловая и электрическая энергия. Именно поэтому любые металлы отличаются такой особенностью, как проводимость.

Общие понятия о твердом теле
Твердые тела и вещества - это практически одно и то же. Этими терминами называют одно из 4 агрегатных состояний. Твердые тела имеют стабильную форму и характер теплового движения атомов. Причем последние совершают малые колебания рядом с положениями равновесия. Раздел науки, занимающийся изучением состава и внутренней структуры, называют физикой твердого тела. Существуют и другие важные области знаний, занимающиеся такими веществами. Изменение формы при внешних воздействиях и движении называют механикой деформируемого тела.
Благодаря различным свойствам твердых веществ они нашли применение в разных технических приспособлениях, созданных человеком. Чаще всего в основе их употребления лежали такие свойства, как твердость, объем, масса, упругость, пластичность, хрупкость. Современная наука позволяет использовать и другие качества твердых веществ, которые можно обнаружить исключительно в лабораторных условиях.
Что такое кристаллы
Кристаллы - это твердые тела с расположенными в определенном порядке частицами. Каждому соответствует своя структура. Его атомы образуют трехмерно-периодическую укладку, называемую кристаллической решеткой. Твердые вещества обладают различной симметрией структуры. Кристаллическое состояние твердого тела считается устойчивым, поскольку имеет минимальное количество потенциальной энергии.
Подавляющее большинство твердых состоит из огромного числа беспорядочно ориентированных отдельных зерен (кристаллитов). Такие вещества называют поликристаллическими. К ним относят технические сплавы и металлы, а также множество горных пород. Монокристаллическими называют одиночные природные или синтетические кристаллы.
Чаще всего такие твердые тела образуются из состояния жидкой фазы, представленного расплавом или раствором. Иногда их получают и из газообразного состояния. Этот процесс называют кристаллизацией. Благодаря научно-техническому прогрессу процедура выращивания (синтеза) различных веществ получила промышленный масштаб. Большинство кристаллов имеет естественную форму в виде Их размеры бывают самыми разными. Так, природный кварц (горный хрусталь) может весить до сотен килограммов, а алмазы - до нескольких грамм.

В аморфных твердых телах атомы находятся в постоянном колебании вокруг хаотически находящихся точек. В них сохраняется определенный ближний порядок, но отсутствует дальний. Это обусловлено тем, что их молекулы расположены на расстоянии, которое можно сравнить с их размером. Наиболее часто встречающимся в нашей жизни примером такого твердого вещества является стеклообразное состояние. часто рассматриваются как жидкость с бесконечно большой вязкостью. Время их кристаллизации иногда так велико, что и вовсе не проявляется.
Именно вышеперечисленные свойства данных веществ делают их уникальными. Аморфные твердые тела считаются нестабильными, поскольку со временем могут перейти в кристаллическое состояние.
Молекулы и атомы, из которых состоит твердое вещество, упакованы с большой плотностью. Они практически сохраняют свое взаимоположение относительно иных частиц и держатся вместе благодаря межмолекулярному взаимодействию. Расстояние между молекулами твердого вещества в различных направлениях именуют параметром кристаллической решетки. Структура вещества и ее симметричность определяют множество свойств, таких как электронная зона, спайность и оптика. При воздействии на твердое вещество достаточно большой силы эти качества могут быть в той или иной степени нарушены. При этом твердое тело поддается остаточной деформации.
Атомы твердых тел совершают колебательные движения, которыми обусловлено обладание ими тепловой энергией. Поскольку они ничтожно малы, их можно наблюдать только при лабораторных условиях. твердого вещества во многом влияет на его свойства.

Изучение твердых веществ
Особенности, свойства данных веществ, их качества и движение частиц изучаются различными подразделами физики твердого тела.
Для исследования используются: радиоспектроскопия, структурный анализ при помощи рентгена и другие методы. Так изучаются механические, физические и тепловые свойства твердых веществ. Твердость, сопротивление нагрузкам, предел прочности, фазовые превращения изучает материаловедение. Оно в значительной степени перекликается с физикой твердых тел. Существует и другая важная современная наука. Исследование существующих и синтезирование новых веществ проводятся химией твердого состояния.
Особенности твердых веществ
Характер движения внешних электронов атомов твердого вещества определяет многие его свойства, например, электрические. Существует 5 классов таких тел. Они установлены в зависимости от типа связи атомов:
- Ионная, основной характеристикой которой является сила электростатического притяжения. Ее особенности: отражение и поглощение света в инфракрасной области. При малой температуре ионная связь отличается малой электропроводностью. Примером такого вещества является натриевая соль соляной кислоты (NaCl).
- Ковалентная, осуществляемая за счет электронной пары, которая принадлежит обоим атомам. Такая связь подразделяется на: одинарную (простую), двойную и тройную. Эти названия говорят о наличии пар электронов (1, 2, 3). Двойные и тройные связи называют кратными. Существует еще одно деление этой группы. Так, в зависимости от распределения электронной плотности выделяют полярную и неполярную связь. Первая образуется разными атомами, а вторая - одинаковыми. Такое твердое состояние вещества, примеры которого - алмаз (С) и кремний (Si), отличается своей плотностью. Самые твердые кристаллы относятся именно к ковалентной связи.
- Металлическая, образующаяся путем объединения валентных электронов атомов. В результате чего возникает общее электронное облако, которое смещается под воздействием электрического напряжения. Металлическая связь образуется тогда, когда связываемые атомы большие. Именно они способны отдавать электроны. У многих металлов и сложных соединений данной связью образуется твердое состояние вещества. Примеры: натрий, барий, алюминий, медь, золото. Из неметаллических соединений можно отметить следующие: AlCr 2 , Ca 2 Cu, Cu 5 Zn 8 . Вещества с металлической связью (металлы) разнообразны по физическим свойствам. Они могут быть жидкими (Hg), мягкими (Na, K), очень твердыми (W, Nb).
- Молекулярная, возникающая в кристаллах, которые образуются отдельными молекулами вещества. Ее характеризуют промежутки между молекулами с нулевой электронной плотностью. Силы, связывающие атомы в таких кристаллах, значительны. При этом молекулы притягиваются друг к другу только слабым межмолекулярным притяжением. Именно поэтому связи между ними легко разрушаются при нагревании. Соединения между атомами разрушаются намного сложнее. Молекулярная связь подразделяется на ориентационную, дисперсионную и индукционную. Примером такого вещества является твердый метан.
- Водородная, которая возникает между положительно поляризованными атомами молекулы или ее части и отрицательно поляризованной наименьшей частицей иной молекулы либо другой части. К таким связям можно отнести лед.

Свойства твердых веществ
Что нам известно на сегодняшний день? Ученые давно изучают свойства твердого состояния вещества. При воздействии на него температур изменяется и оно. Переход такого тела в жидкость называют плавлением. Трансформация твердого вещества в газообразное состояние называется сублимацией. При понижении температуры происходит кристаллизация твердого тела. Некоторые вещества под действием холода переходят в аморфную фазу. Этот процесс ученые называют стеклованием.
При изменяется внутренняя структура твердых тел. Наибольшую упорядоченность она приобретает при понижении температуры. При атмосферном давлении и температуре Т > 0 К любые вещества, существующие в природе, затвердевают. Только гелий, для кристаллизации которого нужно давление в 24 атм, составляет исключение из этого правила.
Твердое состояние вещества придает ему различные физические свойства. Они характеризуют специфическое поведение тел под воздействием определенных полей и сил. Эти свойства подразделяют на группы. Выделяют 3 способа воздействия, соответствующие 3 видам энергии (механической, термической, электромагнитной). Соответственно им существует 3 группы физических свойств твердых веществ:
- Механические свойства, связанные с напряжением и деформацией тел. По этим критериям твердые вещества делят на упругие, реологические, прочностные и технологические. В покое такое тело сохраняет свою форму, но оно может изменяться под действием внешней силы. При этом его деформация может быть пластической (начальный вид не возвращается), упругой (возвращается в первоначальную форму) или разрушительной (при достижении определенного порога происходит распад/разлом). Отзыв на прилагаемое усилие описывают модулями упругости. Твердое тело сопротивляется не только сжатию, растяжению, но и сдвигам, кручению и изгибам. Прочностью твердого тела называют его свойство сопротивляться разрушению.
- Термические, проявляющиеся при воздействии тепловых полей. Одно из самых важных свойств - температура плавления, при которой тело переходит в жидкое состояние. Оно отмечается у кристаллических твердых веществ. Аморфные тела обладают скрытой теплотой плавления, поскольку их переход в жидкое состояние при повышении температуры происходит постепенно. По достижении определенной теплоты аморфное тело теряет упругость и приобретает пластичность. Это состояние означает достижение им температуры стеклования. При нагревании происходит деформация твердого тела. Причем оно чаще всего расширяется. Количественно это состояние характеризуется определенным коэффициентом. Температура тела влияет на такие механические характеристики, как текучесть, пластичность, твердость и прочность.
- Электромагнитные, связанные с воздействием на твердое вещество потоков микрочастиц и электромагнитных волн большой жесткости. К ним условно относят и радиационные свойства.

Зонная структура
Твердые вещества классифицируются и по так называемой зонной структуре. Так, среди них различают:
- Проводники, отличающиеся тем, что зоны их проводимости и валентности перекрываются. При этом электроны могут перемещаться между ними, получая малейшую энергию. К проводникам относятся все металлы. При приложении к такому телу разности потенциалов образуется электрический ток (благодаря свободному передвижению электронов между точками с наименьшим и большим потенциалом).
- Диэлектрики, зоны которых не перекрываются. Интервал между ними превышает 4 эВ. Для проведения электронов из валентной в проводимую зону необходима большая энергия. Благодаря таким свойствам диэлектрики практически не проводят ток.
- Полупроводники, характеризующиеся отсутствием зон проводимости и валентности. Интервал между ними меньше 4 эВ. Для перевода электронов из валентной в проводимую зону необходима энергия меньшая, чем для диэлектриков. Чистые (нелегированные и собственные) полупроводники плохо пропускают ток.
Движения молекул в твердых веществах обуславливают их электромагнитные свойства.
Другие свойства
Твердые тела подразделяются и по своим магнитным свойствам. Есть три группы:
- Диамагнетики, свойства которых мало зависят от температуры или агрегатного состояния.
- Парамагнетики, являющиеся следствием ориентации электронов проводимости и магнитных моментов атомов. Согласно закону Кюри, их восприимчивость убывает пропорционально температуре. Так, при 300 К она составляет 10 -5 .
- Тела с упорядоченной магнитной структурой, обладающие дальним порядком атомов. В узлах их решетки периодически располагаются частицы с магнитными моментами. Такие твердые тела и вещества часто используются в разных сферах деятельности человека.

Самые твердые вещества в природе
Какие же они? Плотность твердых веществ во многом определяет их твердость. За последние годы ученые открыли несколько материалов, которые претендуют на звание «наиболее прочного тела». Самое твердое вещество - это фуллерит (кристалл с молекулами фуллерена), который примерно в 1,5 раза тверже алмаза. К сожалению, он пока доступен только в крайне малых количествах.
На сегодняшний день самое твердое вещество, которое в дальнейшем, возможно, будет использоваться в промышленности, - лонсдейлит (гексагональный алмаз). Он на 58% тверже бриллианта. Лонсдейлит - аллотропная модификация углерода. Его кристаллическая решетка очень напоминает алмазную. Ячейка лонсдейлита содержит 4 атома, а бриллианта - 8. Из широко используемых кристаллов на сегодня самым твердым остается алмаз.
Физика. Молекулы. Расположение молекул в газообразном, жидком и твердом расстоянии.
- В газообразном состоянии молекулы не связаны друг с другом, находятся на большом расстоянии друг от друга. Движение Броуновское. Газ может быть относительно легко сжат.
В жидком - молекулы близко друг к другу, колеблются вместе. Сжатию почти не поддаются.
В тврдом - молекулы расположены в строгом порядке (в кристаллических рештках), всякое движение молекул отсутствует. Сжатию не поддатся. - Строение вещества и начала химии:
http://samlib.ru/a/anemow_e_m/aa0.shtml
(без регистрации и SMS-сообщений, в удобном текстовом формате: можно использовать Ctrl+C) - Никак нельзя согласиться с тем, что в твердом состоянии молекулы не движутся.
Движение молекул в газах
В газах обычно расстояние между молекулами и атомами значительно больше размеров молекул, а силы притяжения очень малы. Поэтому газы не имеют собственной формы и постоянного объма. Газы легко сжимаются, потому что силы отталкивания на больших расстояниях также малы. Газы обладают свойством неограниченно расширяться, заполняя весь предоставленный им объм. Молекулы газа движутся с очень большими скоростями, сталкиваются между собой, отскакивают друг от друга в разные стороны. Многочисленные удары молекул о стенки сосуда создают давление газа.
Движение молекул в жидкостях
В жидкостях молекулы не только колеблются около положения равновесия, но и совершают перескоки из одного положения равновесия в соседнее. Эти перескоки происходят периодически. Временной отрезок между такими перескоками получил название среднее время оседлой жизни (или среднее время релаксации) и обозначается буквой?. Иными словами, время релаксации это время колебаний около одного определнного положения равновесия. При комнатной температуре это время составляет в среднем 10-11 с. Время одного колебания составляет 10-1210-13 с.
Время оседлой жизни уменьшается с повышением температуры. Расстояние между молекулами жидкости меньше размеров молекул, частицы расположены близко друг к другу, а межмолекулярное притяжение велико. Тем не менее, расположение молекул жидкости не является строго упорядоченным по всему объму.
Жидкости, как и тврдые тела, сохраняют свой объм, но не имеют собственной формы. Поэтому они принимают форму сосуда, в котором находятся. Жидкость обладает таким свойством, как текучесть. Благодаря этому свойству жидкость не сопротивляется изменению формы, мало сжимается, а е физические свойства одинаковы по всем направлениям внутри жидкости (изотропия жидкостей). Впервые характер молекулярного движения в жидкостях установил советский физик Яков Ильич Френкель (1894 1952).
Движение молекул в тврдых телах
Молекулы и атомы тврдого тела расположены в определнном порядке и образуют кристаллическую рештку. Такие тврдые вещества называют кристаллическими. Атомы совершают колебательные движения около положения равновесия, а притяжение между ними очень велико. Поэтому тврдые тела в обычных условиях сохраняют объм и имеют собственную форм
- В газообразном-движутся рандомно, врубаются
В жидком-движутся в соответствии друг с другом
В твердом - не движутся.
Рассмотрим, как меняется в зависимости от расстояния между молекулами проекция результирующей силы взаимодействия между ними на прямую, соединяющую центры молекул. Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия между ними практически не сказываются. Силы взаимодействия между молекулами короткодействующие.
На расстояниях, превышающих 2-3 диаметра молекул, сила отталкивания практически равна нулю. Заметна лишь сила притяжения. По мере уменьшения расстояния сила притяжения возрастает и одновременно начинает сказываться сила отталкивания. Эта сила очень быстро увеличивается, когда электронные оболочки молекул начинают перекрываться.
На рисунке 2.10 графически изображена зависимость проекции F r силы взаимодействия молекул от расстояния между их центрами. На расстоянии r 0 , примерно равном сумме радиусов молекул, F r = 0 , так как сила притяжения равна по модулю силе отталкивания. При r > r 0 между молекулами действует сила притяжения. Проекция силы, действующей на правую молекулу, отрицательна. При r < r 0 действует сила отталкивания с положительным значением проекции F r .
Происхождение сил упругости
Зависимость сил взаимодействия молекул от расстояния между ними объясняет появление силы упругости при сжатии и растяжении тел. Если пытаться сблизить молекулы на расстояние, меньшее г0, то начинает действовать сила, препятствующая сближению. Наоборот, при удалении молекул друг от друга действует сила притяжения, возвращающая молекулы в исходные положения после прекращения внешнего воздействия.
При малом смещении молекул из положений равновесия силы притяжения или отталкивания растут линейно с увеличением смещения. На малом участке кривую можно считать отрезком прямой (утолщенный участок кривой на рис. 2.10). Именно поэтому при малых деформациях оказывается справедливым закон Гука, согласно которому сила упругости пропорциональна деформации. При больших смещениях молекул закон Гука уже несправедлив.
Так как при деформации тела изменяются расстояния между всеми молекулами, то на долю соседних слоев молекул приходится незначительная часть общей деформации. Поэтому закон Гука выполняется при деформациях, в миллионы раз превышающих размеры молекул.
Атомно-силовой микроскоп
На действии сил отталкивания между атомами и молекулами на малых расстояниях основано устройство атомно-силового микроскопа (АСМ). Этот микроскоп в отличие от туннельного позволяет получать изображения не проводящих электрический ток поверхностей. Вместо вольфрамового острия в АСМ используют маленький осколок алмаза, заостренный до атомных размеров. Этот осколок закрепляется на тонком металлическом держателе. При сближении острия с исследуемой поверхностью электронные облака атомов алмаза и поверхности начинают перекрываться и возникают силы отталкивания. Эти силы отклоняют кончик алмазного острия. Отклонение регистрируется с помощью лазерного луча, отражающегося от зеркальца, закрепленного на держателе. Отраженный луч приводит в действие пьезоэлектрический манипулятор, аналогичный манипулятору туннельного микроскопа. Механизм обратной связи обеспечивает такую высоту алмазной иглы над поверхностью, чтобы изгиб пластины держателя оставался неизменным.
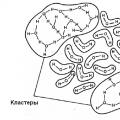
На рисунке 2.11 вы видите изображение полимерных цепей аминокислоты аланина, полученное с помощью АСМ. Каждый бугорок представляет собой одну молекулу аминокислоты.

В настоящее время сконструированы атомные микроскопы, устройство которых основано на действии молекулярные сил притяжения на расстояниях, в несколько раз превышающих размеры атома. Эти силы примерно в 1000 раз меньше сил отталкивания в АСМ. Поэтому применяется более сложная чувствительная система для регистрации сил.
Атомы и молекулы состоят из электрически заряженных частиц. Благодаря действию электрических сил на малых расстояниях молекулы притягиваются, но начинают отталкиваться, когда электронные оболочки атомов перекрываются.
Многие явления природы свидетельствуют о хаотичном движении микрочастиц, молекул и атомов вещества. Чем выше температура вещества, тем более интенсивно это движение. Поэтому теплота тела является отражением беспорядочного движения составляющих его молекул и атомов.
Доказательством того, что все атомы и молекулы вещества находятся в постоянном и беспорядочном движении, может служить диффузия – взаимопроникновение частиц одного вещества в другое (см. рис. 20а). Так, запах быстро распространяется по комнате даже при отсутствии движения воздуха. Капля чернил быстро делает весь стакан с водой однородно чёрным, хотя, казалось бы, сила тяжести должна помогать окрашивать стакан только в направлении сверху-вниз. Диффузию можно обнаружить и в твёрдых телах, если прижать их плотно друг к другу и оставить на длительное время. Явление диффузии демонстрирует, что микрочастицы вещества способны самопроизвольно двигаться во все стороны. Такое движение микрочастиц вещества, а также его молекул и атомов, называют их тепловым движением.
Очевидно, что все молекулы воды в стакане движутся даже, если в нём нет капли чернил. Просто, диффузия чернил делает тепловое движение молекул заметным. Другим явлением, позволяющим наблюдать за тепловым движением и даже оценивать его характеристики, может служить броуновское движение, которым называют видимое в микроскоп хаотическое движение любых мельчайших частичек в совершенно спокойной жидкости. Броуновским оно было названо в честь английского ботаника Р. Броуна, который в 1827 году, рассматривая в микроскоп взвешенные в воде споры пыльцы одного из растений, обнаружил, что они непрерывно и хаотически движутся.
Наблюдение Броуна подтвердили многие другие ученые. Оказалось, что броуновское движение не связано ни с потоками в жидкости, ни с ее постепенным испарением. Мельчайшие частички (их тоже назвали броуновскими) вели себя, как живые, и этот «танец» частиц ускорялся с нагревом жидкости и с уменьшением размера частиц и, наоборот, замедлялся при замене воды на более вязкую среду. Особенно заметным было броуновское движение, когда его наблюдали в газе, например, следили за частичками дыма или капельками тумана в воздухе. Это удивительное явление никогда не прекращалось, и его можно было наблюдать сколь угодно долго.
Объяснение броуновского движения было дано только в последней четверти XIX века, когда многим ученым стало очевидно, что движение броуновской частицы вызвано беспорядочными ударами молекул среды (жидкости или газа), совершающих тепловое движение (см. рис. 20б). В среднем, молекулы среды воздействуют на броуновскую частицу со всех сторон с равной силой, однако, эти удары никогда в точности не уравновешивают друг друга, и в результате, скорость броуновской частицы беспорядочно меняется по величине и направлению. Поэтому броуновская частица движется по зигзагообразному пути. При этом, чем меньше размеры и масса броуновской частицы, тем более заметным становится её движение.
В 1905 году А. Эйнштейн создал теорию броуновского движения, считая, что в каждый данный момент времени ускорение броуновской частицы зависит от числа соударений с молекулами среды, а значит, оно зависит от числа молекул в единице объема среды, т.е. от числа Авогадро. Эйнштейн вывел формулу, по которой можно было вычислить, как изменяется средний квадрат перемещения броуновской частицы со временем, если знать температуру среды, её вязкость, размер частицы и число Авогадро, которое в то время ещё было неизвестно. Справедливость этой теории Эйнштейна была подтверждена экспериментально Ж. Перреном, который первым и получил значение числа Авогадро. Таким образом, анализ броуновского движения заложил основы современной молекулярно-кинетической теории строения вещества.
Вопросы для повторения:
· Что такое диффузия, и как она связана с тепловым движением молекул?
· Что называют броуновским движением, и является ли оно тепловым?
· Как изменяется характер броуновского движения при нагревании?
Рис. 20. (а) – в верхней части показаны молекулы двух различных газов, разделённых перегородкой, которую убирают (см. нижнюю часть), после чего начинается диффузия; (б) в левой нижней части показано схематическое изображение броуновской частицы (синяя), окружённой молекулами среды, столкновения с которыми являются причиной движения частицы (см. три траектории движения частицы).
§ 21. МЕЖМОЛЕКУЛЯРНЫЕ СИЛЫ: СТРОЕНИЕ ГАЗООБРАЗНЫХ, ЖИДКИХ И ТВЁРДЫХ ТЕЛ
Мы привыкли к тому, что жидкость можно перелить из одного сосуда в другой, а газ быстро заполняет весь предоставленный ему объём. Вода может течь только вдоль русла реки, а воздух над ней не знает границ. Если бы газ не стремился занять всё пространство вокруг, мы бы задохнулись, т.к. выдыхаемый нами углекислый газ скапливался бы около нас, не давая нам сделать глоток свежего воздуха. Да, и автомобили бы скоро остановились по той же причине, т.к. для сгорания топлива им тоже нужен кислород.
Почему же газ, в отличие от жидкости, заполняет весь предоставленный ему объём? Между всеми молекулами действует межмолекулярные силы притяжения, величина которых очень быстро падает с удалением молекул друг от друга, и поэтому на расстоянии, равном нескольким диаметрам молекул, они вообще не взаимодействуют. Легко показать, что расстояние между соседними молекулами газа во много раз больше, чем у жидкости. Используя формулу (19.3) и зная плотность воздуха (r=1,29 кг/м3) при атмосферном давлении и его молярную массу (M=0,029 кг/моль), можно вычислить среднее расстояние между молекулами воздуха, которое окажется равным 6,1.10-9 м, что в двадцать раз превышает расстояние между молекулами воды.
Таким образом, между молекулами жидкости, расположенными почти вплотную друг к другу, действуют силы притяжения, препятствующие этим молекулам разлететься в разные стороны. Наоборот, ничтожные силы притяжения между молекулами газа не в состоянии удержать их вместе, и поэтому газы могут расширяться, заполняя весь предоставленный им объём. В существовании межмолекулярных сил притяжения можно убедиться, поставив простой опыт – прижать друг к другу два свинцовых бруска. Если поверхности соприкосновения будут достаточно гладкими, то бруски слипнутся, и их будет тяжело разъединить.
Однако межмолекулярные силы притяжения одни не могут объяснить все различия между свойствами газообразных, жидких и твёрдых веществ. Почему, например, уменьшить объём жидкости или твёрдого тела очень тяжело, а сжать воздушный шарик относительно легко? Объясняется это тем, что между молекулами существуют не только силы притяжения, но и межмолекулярные силы отталкивания, действующие тогда, когда электронные оболочки атомов соседних молекул начинают перекрываться. Именно эти силы отталкивания препятствуют тому, чтобы одна молекула не проникала в объём, уже занятый другой молекулой.
Когда на жидкое или твёрдое тело не действуют внешние силы, расстояние между их молекулами такое (см. r0 на рис.21а), при котором результирующая сил притяжения и отталкивания равна нулю. Если пытаться уменьшить объём тела, то расстояние между молекулами уменьшается, и со стороны сжатого тела начинает действовать результирующая возросших сил отталкивания. Наоборот, при растяжении тела возникающие силы упругости связаны с относительным ростом сил притяжения, т.к. при отдалении молекул друг от друга силы отталкивания падают гораздо быстрее, чем силы притяжения (см. рис.21а).
Молекулы газов находятся на расстояниях в десятки раз больших, чем их размеры, в результате чего эти молекулы не взаимодействуют между собой, и поэтому газы гораздо легче сжимаются, чем жидкости и твёрдые тела. Газы не имеют какой-либо определённой структуры и представляют собой совокупность движущихся и сталкивающихся молекул (см. рис. 21б).
Жидкость – это совокупность молекул, почти вплотную прилегающих друг к другу (см. рис. 21в). Тепловое движение позволяет молекуле жидкости время от времени менять своих соседей, перескакивая с одного места на другое. Этим и объясняется текучесть жидкостей.
Атомы и молекулы твёрдых тел лишены возможности менять своих соседей, а их тепловое движение – это лишь небольшие колебания относительно положения соседних атомов или молекул (см. рис. 21г). Взаимодействие между атомами может приводить к тому, что твёрдое вещество становится кристаллом, а атомы в нём занимают положения в узлах кристаллической решётки. Так как молекулы твёрдых тел не движутся относительно соседей, то эти тела сохраняют свою форму.
Вопросы для повторения:
· Почему молекулы газа не притягиваются друг к другу?
· Какие свойства тел определяют межмолекулярные силы отталкивания и притяжения?
· Как объясняют текучесть жидкости?
· Почему все твёрдые тела сохраняют свою форму?

§ 22. ИДЕАЛЬНЫЙ ГАЗ. ОСНОВНОЕ УРАВНЕНИЕ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ.
Молекулярно-кинетическая теория даёт объяснение тому, что все вещества могут находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. Например, лёд, вода и водяной пар. Часто плазму считают четвёртым состоянием вещества.
Агрегатные состояния вещества (от латинского aggrego – присоединяю, связываю) – состояния одного и того же вещества, переходы между которыми сопровождаются изменением его физических свойств. В этом и заключается изменение агрегатных состояний вещества.
Во всех трёх состояниях молекулы одного и того же вещества ничем не отличаются друг от друга, меняется только их расположение, характер теплового движения и силы межмолекулярного взаимодействия.
Движение молекул в газах
В газах обычно расстояние между молекулами и атомами значительно больше размеров молекул, а силы притяжения очень малы. Поэтому газы не имеют собственной формы и постоянного объёма. Газы легко сжимаются, потому что силы отталкивания на больших расстояниях также малы. Газы обладают свойством неограниченно расширяться, заполняя весь предоставленный им объём. Молекулы газа движутся с очень большими скоростями, сталкиваются между собой, отскакивают друг от друга в разные стороны. Многочисленные удары молекул о стенки сосуда создают давление газа .
Движение молекул в жидкостях
В жидкостях молекулы не только колеблются около положения равновесия, но и совершают перескоки из одного положения равновесия в соседнее. Эти перескоки происходят периодически. Временной отрезок между такими перескоками получил название среднее время оседлой жизни (или среднее время релаксации ) и обозначается буквой?. Иными словами, время релаксации – это время колебаний около одного определённого положения равновесия. При комнатной температуре это время составляет в среднем 10 -11 с. Время одного колебания составляет 10 -12 …10 -13 с.
Время оседлой жизни уменьшается с повышением температуры. Расстояние между молекулами жидкости меньше размеров молекул, частицы расположены близко друг к другу, а межмолекулярное притяжение велико. Тем не менее, расположение молекул жидкости не является строго упорядоченным по всему объёму.
Жидкости, как и твёрдые тела, сохраняют свой объём, но не имеют собственной формы. Поэтому они принимают форму сосуда, в котором находятся. Жидкость обладает таким свойством, как текучесть . Благодаря этому свойству жидкость не сопротивляется изменению формы, мало сжимается, а её физические свойства одинаковы по всем направлениям внутри жидкости (изотропия жидкостей). Впервые характер молекулярного движения в жидкостях установил советский физик Яков Ильич Френкель (1894 – 1952).
Движение молекул в твёрдых телах
Молекулы и атомы твёрдого тела расположены в определённом порядке и образуют кристаллическую решётку . Такие твёрдые вещества называют кристаллическими. Атомы совершают колебательные движения около положения равновесия, а притяжение между ними очень велико. Поэтому твёрдые тела в обычных условиях сохраняют объём и имеют собственную форму.
Физика
![]()
![]()
Взаимодействие между атомами и молекулами вещества. Строение твердых, жидких и газообразных тел
Между молекулами вещества действуют одновременно силы притяжения и силы отталкивания. Эти силы в большой степени зависят от расстояний между молекулами.
Согласно экспериментальным и теоретическим исследованиям межмолекулярные силы взаимодействия обратно пропорциональны n-й степени расстояния между молекулами:
где для сил притяжения n = 7, а для сил отталкивания .
Взаимодействие двух молекул можно описать при помощи графика зависимости проекции равнодействующей сил притяжения и отталкивания молекул от расстояния r между их центрами. Направим ось r от молекулы 1, центр которой совпадает с началом координат, к находящемуся от него на расстоянии центру молекулы 2 (рис. 1).

Тогда проекция силы отталкивания молекулы 2 от молекулы 1 на ось r будет положительной. Проекция силы притяжения молекулы 2 к молекуле 1 будет отрицательной.
Силы отталкивания (рис. 2) гораздо больше сил притяжения на малых расстояниях , но гораздо быстрее убывают с увеличением r. Силы притяжения тоже быстро убывают с увеличением r, так что, начиная с некоторого расстояния , взаимодействием молекул можно пренебречь. Наибольшее расстояние rm, на котором молекулы еще взаимодействуют, называется радиусом молекулярного действия ![]() .
.

Силы отталкивания по модулю равны силам притяжения.
Расстояние соответствует устойчивому равновесному взаимному положению молекул.
В различных агрегатных состояниях вещества расстояние между его молекулами различно. Отсюда и различие в силовом взаимодействии молекул и существенное различие в характере движения молекул газов, жидкостей и твердых тел.
В газах расстояния между молекулами в несколько раз превышают размеры самих молекул. Вследствие этого силы взаимодействия между молекулами газа малы и кинетическая энергия теплового движения молекул намного превышает потенциальную энергию их взаимодействия. Каждая молекула движется свободно от других молекул с огромными скоростями (сотни метров в секунду), меняя направление и модуль скорости при столкновениях с другими молекулами. Длина свободного пробега молекул газа зависит от давления и температуры газа. При нормальных условиях .
В жидкостях расстояние между молекулами значительно меньше, чем в газах. Силы взаимодействия между молекулами велики, и кинетическая энергия движения молекул соизмерима с потенциальной энергией их взаимодействия, вследствие чего молекулы жидкости совершают колебания около некоторого положения равновесия, затем скачкообразно переходят в новые положения равновесия через очень малые промежутки времени , что приводит к текучести жидкости. Таким образом, в жидкости молекулы совершают в основном колебательные и поступательные движения. В твердых телах силы взаимодействия между молекулами настолько велики, что кинетическая энергия движения молекул намного меньше потенциальной энергии их взаимодействия. Молекулы совершают лишь колебания с малой амплитудой около некоторого постоянного положения равновесия - узла кристаллической решетки.
Это расстояние можно оценить, зная плотность вещества и молярную массу . Концентрация – число частиц в единице объема, связана с плотностью, молярной массой и числом Авогадро соотношением.